Группа - это одно из ключевых понятий химии, в котором заключаются основные принципы организации элементов в периодической таблице. Именно группы определяют химические свойства элементов и помогают их классифицировать. Запись формулировки периодического закона в химии, связанного с группой, является важным моментом в изучении этой науки.
Периодический закон - это закономерность, согласно которой химические свойства элементов повторяются через определенные промежутки, называемые периодами. Каждая группа элементов имеет свои уникальные свойства, определяющиеся их электронной конфигурацией и валентностью.
Запись формулировки периодического закона в химии, называемого группой, обычно выглядит следующим образом: Группа N, где N - номер группы. Это означает, что элементы данной группы имеют одинаковое количество внешних электронов и, следовательно, схожие химические свойства. Так, например, группа 1 включает щелочные металлы, которые обладают одной валентной электронной оболочкой и проявляют схожие реакции с водой и кислородом.
Периодический закон в химии
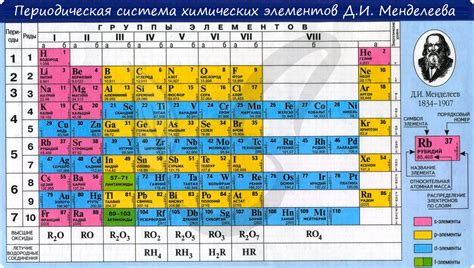
Основная идея периодического закона заключается в том, что свойства элементов повторяются периодически с изменением их атомных номеров. По мере увеличения атомного номера, происходит изменение электронной конфигурации и, как следствие, свойств элементов.
Важными элементами периодической системы являются группы элементов, состоящие из химических элементов с сходными свойствами. Каждая группа имеет свое наименование и характеристики.
- Группа щелочных металлов (1 группа) - это элементы с одним валентным электроном и химически активные свойства.
- Группа щелочноземельных металлов (2 группа) - это элементы со свойствами, близкими к щелочным металлам, но менее активные.
- Группа галогенов (17 группа) - это элементы с высокой электроотрицательностью и химической активностью.
- Группа инертных газов (18 группа) - это элементы с полностью заполненными электронными оболочками и низкой химической активностью.
Периодический закон играет важную роль в понимании и классификации химических элементов, а также в предсказании и изучении их свойств и реакций.
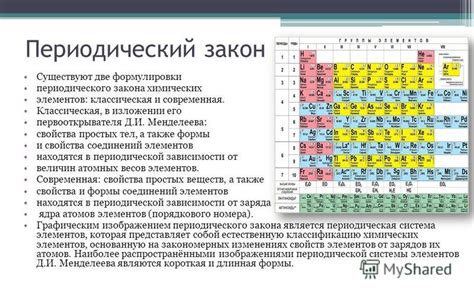
Запись формулировки периодического закона в химии, называемого группой
| Группа | Номер | Название |
|---|---|---|
| 1 | 1 | Группа щелочных металлов |
| 2 | 2 | Группа щелочноземельных металлов |
| 3 | 3-12 | Главные группы элементов |
| 4 | 13-14 | Группа бора и группа углерода |
| 5 | 15 | Группа азота |
| 6 | 16 | Группа кислорода |
| 7 | 17 | Группа галогенов |
| 8 | 18 | Нобелиевская группа |
Периодический закон
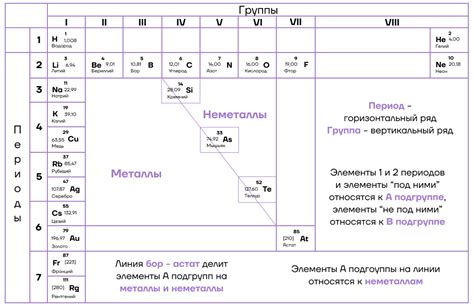
Периодический закон в химии формулирует основные закономерности изменения химических свойств элементов с увеличением их атомного номера в таблице химических элементов.
Закон был открыт и сформулирован в конце XIX века российским химиком Дмитрием Менделеевым. В основе этого закона лежит представление о том, что свойства химических элементов повторяются периодически через определенные интервалы, формируя так называемые группы.
Каждая группа элементов имеет общие характеристики, такие как количество внешних электронов, электрическая проводимость, химическая реактивность и другие свойства. Изучение периодического закона позволяет классифицировать элементы, предсказывать их свойства и исследовать химические реакции.
Периодический закон стал базовым понятием в химической науке и имеет широкие приложения в различных областях, таких как промышленность, фармакология и электроника.
Химический закон
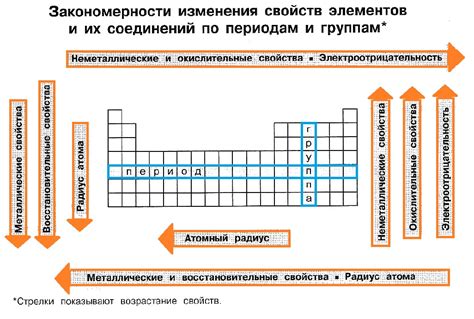
Закон Менделеева был сформулирован русским химиком Дмитрием Ивановичем Менделеевым в 1869 году. Согласно этому закону, свойства химических элементов являются периодическими функциями их атомных номеров. Это означает, что при упорядочении элементов по возрастанию атомных номеров они систематически повторяются с определенным периодом.
Закон Менделеева позволил создать периодическую систему химических элементов, известную как таблица Менделеева. Эта таблица представляет собой удобную и упорядоченную схему, которая позволяет классифицировать и систематизировать все известные химические элементы.
Закон Менделеева имеет большое практическое значение. Он позволяет прогнозировать свойства новых элементов и определять их место в таблице Менделеева. В таблице Менделеева элементы располагаются по горизонтальным рядам, называемым периодами, и вертикальным столбцам, называемым группами.
Каждая группа химических элементов в таблице Менделеева имеет схожие химические и физические свойства. Это объясняется тем, что элементы в одной группе имеют одинаковое число валентных электронов, что влияет на их химическую активность и способность образовывать соединения.
Таким образом, закон Менделеева позволяет систематизировать и классифицировать химические элементы и предсказывать их свойства на основе их положения в таблице Менделеева. Этот закон оказал огромное влияние на развитие химии и представляет собой важный принцип, широко используемый в научных и практических исследованиях.
Новые химические элементы
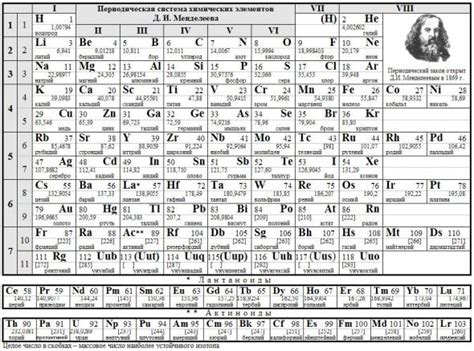
По мере расширения наших знаний о мире вокруг нас, постоянно обнаруживаются новые элементы, которые вносят изменения в таблицу периодических элементов. Каждый новый химический элемент имеет уникальные свойства и может быть использован в различных областях науки и технологий.
Для идентификации и классификации новых элементов используются специальные системы обозначений, основанные на их атомных номерах и химических свойствах. Каждый новый элемент получает своё уникальное название и символ, который затем вписывается в таблицу периодических элементов.
Новые химические элементы открывают перед нами бесконечные возможности для исследования и применения в различных отраслях науки и промышленности. Они позволяют нам лучше понять природу материи и разрабатывать новые материалы и технологии, которые могут изменить нашу жизнь.



