Таблица Менделеева - это один из самых важных инструментов в химии. Она включает в себя все известные элементы и упорядочена по возрастанию атомного номера. Но что означают все эти цифры?
Первая цифра в таблице Менделеева - это атомный номер элемента. Он показывает, сколько протонов содержится в атоме данного элемента. Атомный номер также определяет порядок расположения элементов в таблице. Чем больше атомный номер, тем больше протонов содержится в атоме элемента.
Вторая цифра - это относительная атомная масса элемента. Она показывает, какая масса содержится в атоме данного элемента. Относительная атомная масса определяется сравнением с массой одного атома углерода-12, которой присвоено значение 12 атомных масс. Таким образом, относительная атомная масса элемента указывает, сколько раз его масса больше массы атома углерода-12.
Третья цифра - это группа элемента в таблице. Группы - это вертикальные столбцы (от 1 до 18), в которых располагаются элементы со схожими химическими свойствами. Некоторые группы имеют специальные названия, такие как щелочные металлы, щелочноземельные металлы и благородные газы.
Атомный номер: определяет порядковый номер химического элемента

Атомный номер обозначается символом Z и является одним из основных свойств элемента, которое определяет его положение в периодической системе химических элементов. Атомный номер также определяет реактивность и химические свойства элемента.
Атомный номер имеет важное значение для понимания структуры и свойств атомов и позволяет классифицировать элементы в таблице Менделеева. Чтение таблицы Менделеева становится более удобным, когда известен атомный номер элемента.
Например, атомный номер 1 принадлежит водороду, атомный номер 79 - золоту. Кроме того, атомный номер используется в химических уравнениях и расчетах для определения молярной массы и других характеристик элементов и веществ.
Химический символ: обозначает элемент с использованием одной или двух букв
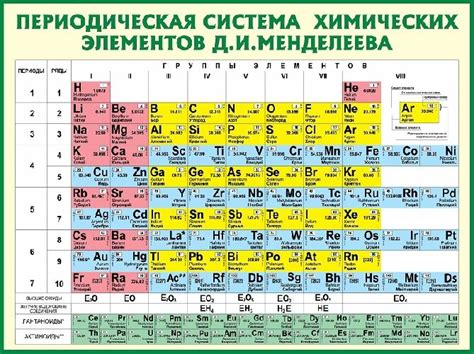
Обычно химический символ соответствует первой букве или первым двум буквам названия элемента на латинском языке. В некоторых случаях, когда первые буквы используются несколькими элементами, добавляется третья буква, чтобы уточнить обозначение.
Например, символ H обозначает водород, символ C - углерод, символ O - кислород. Некоторые элементы имеют символы на основе их латинского названия, например, символы Au (золото) и Fe (железо).
Также в таблице Менделеева есть элементы, у которых символы образованы греческими буквами. Например, символ α означает радиоактивный элемент альфа, символ β - элемент бета, и символ γ - элемент гамма.
Химический символ является важной частью химической номенклатуры и используется в химии и других отраслях науки для обозначения и идентификации элементов.
| Символ | Элемент |
|---|---|
| H | Водород |
| C | Углерод |
| O | Кислород |
| Au | Золото |
| Fe | Железо |
Атомная масса: показывает массу атома элемента в атомных единицах

Атомная масса элемента может быть найдена в таблице Менделеева, где для каждого химического элемента указана его атомная масса. Обычно атомная масса записывается под химическим символом элемента.
Знание атомной массы элемента важно для проведения химических расчетов и определения массового состава соединений. Она также может быть использована для определения количества атомов, молекул и ионов вещества.
Некоторые элементы имеют несколько изотопов, то есть разные атомы с одинаковым количеством протонов, но разным количеством нейтронов. В таких случаях атомная масса указывается в виде среднего значения массы изотопов, где учитывается их относительная распространенность.
Знание атомной массы элемента позволяет ученым и исследователям лучше понять и изучать свойства и реактивность химических элементов.
Период: определяет количество электронных оболочек у элемента

Период в таблице Менделеева указывает на количество электронных оболочек, или энергетических уровней, в атоме элемента. Каждая электронная оболочка может содержать определенное количество электронов.
Периоды в таблице Менделеева пронумерованы от 1 до 7, а каждый период соответствует одной электронной оболочке. Например, элементы первого периода имеют только одну электронную оболочку, элементы второго периода имеют две оболочки, и так далее.
Число электронных оболочек в атоме элемента определяет его химические свойства и реактивность. Элементы с одинаковым числом электронных оболочек находятся в одной вертикальной группе в таблице Менделеева и имеют схожие химические свойства.
Группа: указывает количество электронов на внешней энергетической оболочке
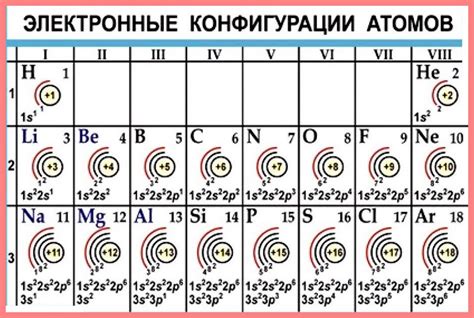
Группа элемента в таблице Менделеева определяет количество электронов, находящихся на внешней энергетической оболочке атома. Всего в таблице Менделеева 18 групп, которые помогают организовать элементы по степени их химической активности.
Количество электронов на внешней оболочке определяет поведение атома в химических реакциях и его способность образовывать связи с другими атомами. Элементы в одной группе имеют одинаковое количество электронов на внешней оболочке и поэтому обладают схожими химическими свойствами.
Например, элементы 1-й группы (группа щелочных металлов), такие как литий, натрий и калий, имеют по одному электрону на внешней оболочке и проявляют подобные химические свойства – они легко образуют ион положительного заряда.
Наоборот, элементы последней группы (группа инертных газов), такие как гелий и неон, имеют полностью заполненную внешнюю оболочку и поэтому не образуют химические связи с другими атомами.
Группа элемента в таблице Менделеева важна для понимания и прогнозирования его химического поведения и связей с другими элементами. Определение группы элемента также помогает классифицировать элементы и упрощает изучение их химических свойств.
Блок: определяет электронную конфигурацию элемента
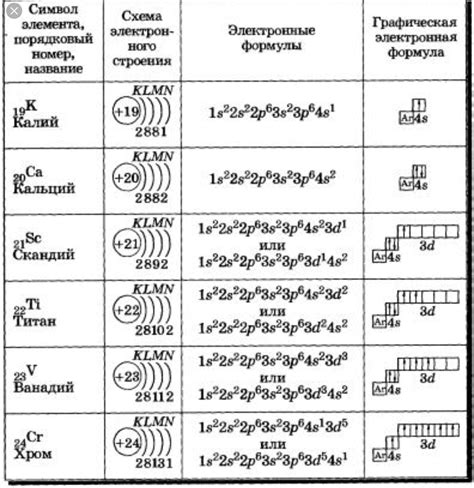
Каждый элемент в таблице Менделеева имеет определенную электронную конфигурацию, которая определяет расположение электронов в его атоме. Электронная конфигурация включает в себя информацию о количестве электронов в каждом энергетическом уровне, а также о их расположении в подуровнях.
Блок элемента в таблице Менделеева указывает на тип элемента. Существуют четыре основных блока:
- С: элементы в s-блоке имеют свои верхние энергетические уровни заполненными электронами s-подуровней. Наиболее известными элементами этого блока являются водород (H) и гелий (He).
- Р: элементы в p-блоке имеют свои верхние энергетические уровни заполненными электронами p-подуровней. К этому блоку относятся такие элементы, как углерод (C), кислород (O) и азот (N).
- d: элементы в d-блоке, также известном как переходные металлы, имеют свои верхние энергетические уровни заполненными электронами d-подуровней. В этот блок входят элементы, такие как железо (Fe), медь (Cu) и цинк (Zn).
- f: элементы в f-блоке, также известном как лантаноиды и актиноиды, имеют свои верхние энергетические уровни заполненными электронами f-подуровней. В этом блоке находятся элементы, такие как лантан (La), уран (U) и плютоний (Pu).
Блок элемента помогает определить его электронную конфигурацию и понять его свойства и химическую активность. Классификация элементов по блокам является важной особенностью таблицы Менделеева и помогает упорядочивать и изучать химические элементы.
Вещество: описывает состояние элемента при обычных условиях
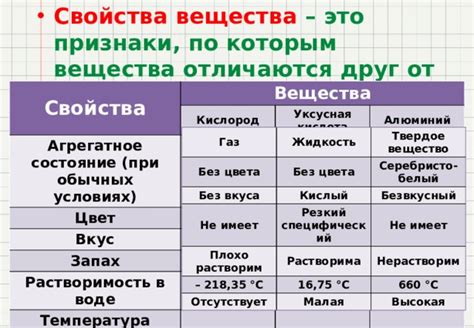
Состояние вещества при обычных условиях может быть газообразным, жидким или твердым. Это зависит от свойств элемента и его атомной структуры. Зная состояние элемента при обычных условиях, мы можем предсказать его поведение и взаимодействие с другими элементами.
В таблице Менделеева кратко указано состояние элемента при обычных условиях. Здесь используются следующие обозначения:
| Газ | Г |
| Жидкость | Ж |
| Твердое вещество | Т |
Например, элемент Литий (Li) имеет обозначение "Т", что означает, что он является твердым веществом при обычных условиях. В то же время, элемент Кислород (O) обозначается как "Г", что означает, что он является газообразным веществом при обычных условиях.
Состояние элемента может изменяться при изменении температуры и давления. Например, некоторые элементы могут переходить из твердого состояния в жидкое или из жидкого в газообразное при повышении температуры или понижении давления. Эти изменения состояния также важны для понимания свойств вещества и его применения в различных областях науки и техники.
Свойства: определяют химические и физические характеристики элемента

Каждый элемент в таблице Менделеева имеет свойство, которое определяет его химические и физические характеристики. Эти свойства помогают ученым понять, как элемент взаимодействует с другими веществами и в каком состоянии он находится при определенных условиях.
Например, атомный номер элемента указывает на количество протонов в его ядре и определяет его положение в таблице Менделеева. Эта характеристика определяет такие свойства, как молекулярная масса, электронная конфигурация и атомный радиус.
Окислительные свойства элемента определяют его способность окислять или восстанавливать другие вещества. Они могут быть выражены через электроотрицательность, которая показывает тенденцию атома притягивать электроны.
Термические и электропроводящие свойства элемента являются результатом его структуры и взаимодействий между атомами. Конкретные значения теплопроводности и электропроводности могут быть различными для разных элементов в таблице Менделеева.
Многие другие свойства, такие как плотность, температура плавления и кипения, также определяются химическими и физическими характеристиками элемента.



