Металлы и сплавы являются основными строительными блоками современного мира. Их уникальные химические свойства и характеристики определяют их множественные применения в различных отраслях промышленности и науки.
Металлы обладают высокой теплопроводностью и электропроводностью, что делает их важными компонентами электрических и теплотехнических устройств. Кроме того, металлы являются долговечными и прочными материалами, что позволяет использовать их в строительстве и производстве машин и оборудования.
Сплавы - это смеси металлов, которые обладают уникальными свойствами, комбинируя преимущества различных материалов. Сплавы часто используются для улучшения прочности и коррозионной стойкости металлов, а также для создания материалов с определенными магнитными, электрическими или химическими свойствами.
Одна из особенностей химических свойств металлов и сплавов - их реактивность. Некоторые металлы, такие как натрий или калий, очень активны химически и реагируют с водой или кислородом воздуха. В то время как другие металлы, такие как золото или платина, являются малореактивными и коррозионно-устойчивыми, что делает их ценными для ювелирных украшений и научных исследований.
Свойства металлов и сплавов

Свойства металлов обусловлены их кристаллической структурой и особенностями связи атомов в кристаллической решетке. Кристаллическая структура металлов позволяет атомам свободно двигаться внутри решетки, благодаря чему металлы обладают пластичностью и деформируемостью.
Металлы имеют высокую плотность, что обусловлено компактностью атомов в кристаллической решетке. Из-за высокой плотности, металлы обладают высокой прочностью и твердостью.
Одной из важных характеристик металлов является их теплопроводность. Металлы хорошо проводят тепло, что делает их эффективными материалами для передачи тепла и кондиционирования воздуха. Этим свойством металлы также обусловлены их использование в производстве котлов и теплообменных установок.
Важным свойством металлов является их электропроводность. Металлы обладают способностью передавать электрический ток благодаря свободным электронам в их кристаллической решетке. Использование металлов в проводниках электрического тока является одним из основных применений металлов в технологии.
Сплавы – это материалы, состоящие из двух или более металлов или металлов и неметаллов. Сплавы обладают уникальными свойствами, которые отличаются от свойств исходных металлов. Сплавами можно изменить физические, механические и химические свойства материалов. Например, добавление небольшого количества другого металла в сплав может повысить его прочность или улучшить его коррозионную стойкость.
- Металлы обладают пластичностью и деформируемостью.
- Металлы имеют высокую прочность и твердость.
- Металлы хорошо проводят тепло.
- Металлы обладают высокой электропроводностью.
Сплавы представляют собой материалы, созданные путем соединения двух или более металлов или металлов с неметаллами. Они обладают уникальными свойствами, отличными от исходных металлов. Сплавы можно настроить для получения определенных свойств, таких как прочность, твердость, термическая стойкость и электропроводность.
Химические характеристики

Кроме того, металлы хорошо реагируют с кислородом, благодаря чему могут образовывать оксиды. Многие из них также активны в реакциях с кислотами, образуя соли и выделяя водород. Чем активнее металл, тем сильнее проявляется его реактивность.
Некоторые металлы, такие как железо, алюминий и цинк, склонны к окислению и коррозии при взаимодействии с окружающей средой. Однако, некоторые металлы, включая золото и платину, обладают высокой химической стойкостью и не подвержены коррозии.
Важным химическим свойством металлов является их способность образовывать сплавы. Сплав - это смесь двух или большего количества металлов. Сплавы могут обладать уникальными свойствами, которые превосходят свойства отдельных металлов. К примеру, сплав бронзы, состоящий из меди и олова, обладает повышенной прочностью и износостойкостью.
Изучение химических характеристик металлов и сплавов позволяет оптимизировать их использование в различных отраслях промышленности, а также способствует разработке новых материалов с улучшенными свойствами.
Металлы и их реакционная способность
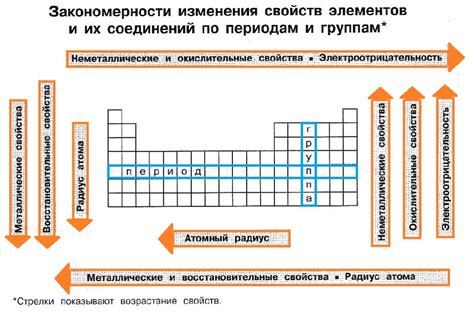
Металлы обладают высокой реакционной способностью, что делает их одними из наиболее важных химических элементов. Их реакционная способность определяется внешней электронной оболочкой, состоящей из валентных электронов.
Металлы проявляют активность в различных химических реакциях. Они имеют способность образовывать ионы положительного заряда, отдавая свои валентные электроны, что позволяет им легко вступать во взаимодействие с отрицательно заряженными частицами.
Одной из самых распространенных реакций металлов является реакция с кислородом воздуха. В результате такой реакции образуется оксид металла, который может быть щелочным, нейтральным или кислотным по своим свойствам. Например, металл натрий реагирует с кислородом, образуя щелочной оксид Na2O, в то время как металл алюминий образует оксид Al2O3, который обладает кислотными свойствами.
Кроме этого, металлы могут вступать в реакцию с различными кислотами. При контакте с кислотной средой металлы отдают свои электроны, образуя ионы металла, а из кислоты выделяются соответствующие ионы водорода. Например, при реакции металла цинка с серной кислотой образуется сульфат цинка и выделяется водородный газ.
Металлы также реагируют с водой, образуя гидроксиды. Некоторые металлы, например натрий и калий, реагируют с водой даже при комнатной температуре, выделяя водород и образуя гидроксиды металла. Другие металлы, например магний и алюминий, реагируют с водой только при нагревании.
Кроме того, металлы могут взаимодействовать с различными неорганическими и органическими соединениями, образуя специфические химические соединения. Их реакционная способность может быть предсказана на основе их электрохимического потенциала, который определяется их положением в ряду активности металлов.
Физические свойства сплавов

Физические свойства сплавов включают в себя такие характеристики, как плотность, теплоемкость, теплопроводность и электропроводность.
Плотность сплавов может быть различной в зависимости от состава и структуры сплава. Обычно сплавы имеют более высокую плотность по сравнению с чистыми металлами. Это связано с добавлением легирующих элементов, которые могут иметь более высокую плотность.
Теплоемкость сплавов также может быть различной и зависит от состава и структуры сплава. Она определяет количество теплоты, которое необходимо передать сплаву, чтобы его температура изменилась на определенное количество. Сплавы, содержащие различные элементы, могут иметь более высокую теплоемкость, чем чистые металлы.
Теплопроводность сплавов зависит от их состава и структуры. Сплавы обычно имеют более низкую теплопроводность по сравнению с чистыми металлами. Это связано с наличием дефектов в структуре сплава, таких как границы зерен и включения других материалов.
Электропроводность сплавов также зависит от их состава и структуры. Сплавы могут иметь более высокую или более низкую электропроводность по сравнению с чистыми металлами в зависимости от содержания различных элементов и их взаимодействия в сплаве. Электропроводность сплавов может находить применение в различных областях, таких как электроника и электрическая промышленность.
Таким образом, физические свойства сплавов зависят от их состава, структуры и взаимодействия различных компонентов в сплаве. Изучение этих свойств позволяет более полно понять и использовать сплавы в различных областях науки и техники.
Роль металлов в химических процессах

Металлы играют важную роль во многих химических процессах благодаря своим уникальным свойствам. Они обладают высокой электропроводностью, теплопроводностью и магнитными свойствами, что делает их незаменимыми в различных отраслях промышленности и научных исследованиях.
Одной из основных ролей металлов в химических процессах является их способность к каталитической активности. Металлы могут ускорять химические реакции, не участвуя в них сами. Это достигается благодаря способности металлов изменять скорость реакций, стимулировать образование переходных состояний и активировать реагенты.
Важную роль металлы играют также в окислительно-восстановительных реакциях. Они могут служить как окислителями, так и восстановителями в реакциях переноса электронов. Это связано с возможностью металлов взаимодействовать с электронами и образовывать различные степени окисления.
Другой важной ролью металлов в химических процессах является их способность формировать комплексные соединения. Металлы могут образовывать соединения с различными лигандами, такими как вода, аммиак, карбонаты и другие. Эти соединения обладают разнообразными свойствами и находят применение в различных областях, от катализа до медицины.
Металлы также играют важную роль в электрохимических процессах. Они являются основными компонентами электродов в аккумуляторах, электролизеров и других устройствах. Металлы, такие как цинк, железо и медь, способны образовывать ионные соединения и проводить электрический ток.
- Металлы играют важную роль в катализе и ускорении химических реакций.
- Они способны участвовать в окислительно-восстановительных реакциях.
- Металлы формируют комплексные соединения с различными лигандами.
- Они являются основными компонентами электродов в электрохимических процессах.
Коррозия металлов

Коррозия обусловлена химическими реакциями между металлом и окружающей его средой. Основные факторы, влияющие на коррозию, включают влажность, наличие кислорода, агрессивные газы и жидкости, а также температуру. Результатом коррозии часто является образование окислов, гидроксидов и других нестабильных соединений на поверхности металла, что приводит к его разрушению.
Для защиты металлов от коррозии используются различные методы. Одним из самых распространенных способов является нанесение защитных покрытий на поверхность металла, таких как краска или лак. Также применяется гальваническая защита, при которой металлы, имеющие различные потенциалы, соединяются в электролитическую цепь с использованием анодов и катодов.
Особенно подвержены коррозии такие металлы, как железо, сталь, алюминий и цинк. Однако некоторые сплавы, такие как нержавеющая сталь и алюминиевые сплавы с магнием, обладают повышенной стойкостью к коррозии благодаря образованию пассивной оксидной пленки на их поверхности.
Реакционная способность сплавов
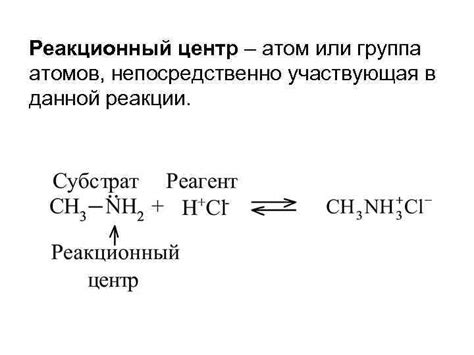
Реакционная способность сплавов обусловлена как химическими свойствами металлов, входящих в сплав, так и структурой и составом самого сплава.
Взаимодействие сплавов происходит с различными элементами и соединениями, как в газовой, так и в жидкой фазе. Для каждого сплава характерны определенные реакции с окружающей средой.
Одним из основных факторов, влияющих на реакционную способность сплавов, является электрохимический потенциал металлов в сплаве. Если металлы в сплаве имеют различные электрохимические потенциалы, то могут возникать электрохимические пары между ними, что приводит к коррозии сплава.
Реакционная способность сплавов также зависит от рН среды, в которой они находятся. В кислой среде некоторые сплавы могут быть устойчивыми и не испытывать коррозии, однако в щелочной или солевой среде они могут быть подвержены растворению или окислению.
Различные элементы, добавленные в сплав, могут значительно повысить его реакционную способность. Например, добавление к сплаву активной металлической пудры может привести к более интенсивному реагированию сплава с воздухом или водой.
Выбор сплава для конкретных условий эксплуатации зависит от его реакционной способности. При проектировании и выборе сплава необходимо учитывать его химическую стойкость и устойчивость к различным реактивам, с которыми он может контактировать в процессе эксплуатации.
Взаимодействие металлов с окружающей средой

Некоторые металлы, такие как железо, алюминий и магний, обладают высокой склонностью к окислению и быстро покрываются тонким слоем оксида. Этот процесс может привести к образованию ржавчины на поверхности металла и его последующему разрушению.
С другой стороны, некоторые металлы, например, золото и платина, обладают высокой устойчивостью к окислению и не образуют оксидной пленки при взаимодействии с воздухом. Это делает их устойчивыми к коррозии и сохраняет их блеск и металлический вид.
Окружающая среда также может влиять на свойства и характеристики металлов. Например, влажность и наличие солей в воздухе могут ускорить процесс коррозии металлов, особенно при наличии проводящей среды, такой как вода или растворы. Некоторые металлы, такие как алюминий и медь, особенно подвержены коррозии в таких условиях.
Также важно отметить, что металлы могут взаимодействовать не только с воздухом, но и с другими веществами окружающей среды. Например, некоторые металлы могут реагировать с водой или кислотами, что приводит к образованию соответствующих солей или газов.
Взаимодействие металлов с окружающей средой является сложным процессом, который зависит от множества факторов, включая тип металла, условия окружающей среды, наличие других химических веществ и т.д. Изучение этих взаимодействий позволяет более полно понять и оценить свойства и характеристики металлов и сплавов.



