Вещества - это материя, состоящая из атомов или молекул, которые обладают определенными химическими свойствами. Существуют два основных типа веществ: молекулярное и немолекулярное.
Молекулярное вещество состоит из двух или более атомов, связанных между собой химическими связями. Эти молекулы могут быть одинаковыми или разными по своему составу. Примером молекулярного вещества является вода (H2O), состоящая из двух атомов водорода и одного атома кислорода, связанных с помощью ковалентных связей.
Немолекулярное вещество представляет собой материю, состоящую из атомов, не связанных между собой. В данном случае, атомы имеют определенные химические свойства индивидуально и они не формируют молекулы. Примером немолекулярного вещества является газовый элементарный кислород (O2), состоящий из двух атомов кислорода, свободных от химической связи.
Основной разницей между молекулярными и немолекулярными веществами является тип связей между атомами. В молекулярных веществах, атомы связаны с помощью ковалентных связей, что происходит при обмене электронами между атомами. В немолекулярных веществах, атомы никак не связаны и не образуют молекулы.
В этой статье мы рассмотрим дополнительные особенности молекулярного и немолекулярного вещества, а также их роль в ежедневной жизни и промышленности.
Молекулярные вещества: что это такое?
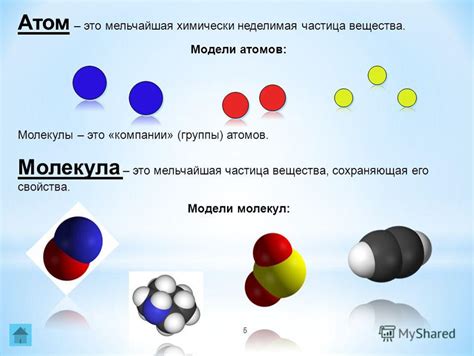
Молекулы молекулярных веществ могут быть составлены из одного или нескольких атомов. Каждый атом в молекуле участвует в образовании химической связи, что позволяет молекуле образовываться и функционировать как одно целое.
Молекулярные вещества могут быть чистыми или смешанными. Чистые молекулярные вещества представляют собой вещества, состоящие только из одного вида молекул, например, кислород или вода. Смешанные молекулярные вещества состоят из различных видов молекул, например, сахар или масло.
Молекулярные вещества имеют ряд особенностей. Они обычно обладают низкими точками плавления и кипения по сравнению с немолекулярными веществами. Также они имеют слабые межмолекулярные силы, что делает их более мягкими и легкими для разрыва связей.
Молекулярные вещества широко распространены в природе и используются людьми в различных сферах жизни. Они могут быть использованы в фармацевтике, пищевой промышленности, электронике и других отраслях. Понимание молекулярных веществ и их свойств позволяет разрабатывать новые материалы, лекарства и улучшать существующие технологии.
Молекулярное строение веществ: особенности и свойства
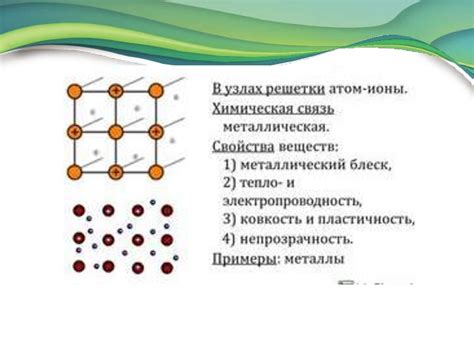
Молекулярное строение вещества объясняет его физические и химические свойства. Молекулы вещества состоят из атомов, связанных между собой химическими связями. Различные вещества могут иметь разные типы и способы связывания атомов.
Особенности молекулярного строения вещества могут включать размеры и формы молекул, наличие двойных или тройных связей, различные функциональные группы и их расположение в структуре молекулы.
Молекулярное строение также может влиять на физические свойства вещества, такие как температура плавления и кипения, теплопроводность, плотность и вязкость. Например, молекулы с большим размером или сложной структурой могут иметь более высокую температуру плавления и кипения.
Химические свойства вещества также связаны с его молекулярным строением. Например, наличие определенных функциональных групп в структуре молекулы может определять ее реакционную способность. Также молекулярное строение может влиять на растворимость вещества, его способность реагировать с другими веществами и образование структурных изомеров.
- Молекулярное строение может быть определено с использованием различных методов: рентгеноструктурный анализ, спектроскопия, масс-спектрометрия и другие.
- Различные вещества могут иметь молекулярное строение разной сложности, что определяет их свойства и применение в различных областях науки и технологий.
Изучение молекулярного строения вещества играет важную роль в химии, физике, биологии и многих других научных областях для понимания его свойств и взаимодействий с другими веществами.
Немолекулярные вещества: понятие и примеры

Примеры немолекулярных веществ включают:
| Вещество | Описание |
| Атомарный кислород (O) | Неметалл, газообразное вещество при комнатной температуре и давлении, играет важную роль в дыхании организмов |
| Йод (I) | Химический элемент, галоген, существует в виде фиолетовых кристаллов, имеет антибактериальные свойства и используется в медицине |
| Фуллерен (C60) | Молекула, состоящая из 60 атомов углерода, имеет форму сферы и используется в нанотехнологиях и медицине |
| Шестиугольный графен (C6) | Однослойный графит, состоящий из шестиугольных ячеек атомов углерода, обладает уникальными электрофизическими свойствами |
Немолекулярные вещества отличаются от молекулярных своим строением и свойствами. Они имеют особую структуру, которая влияет на их физические и химические свойства. Понимание и изучение немолекулярных веществ имеет важное значение для различных областей науки и промышленности.
Сравнение молекулярных и немолекулярных веществ: различия
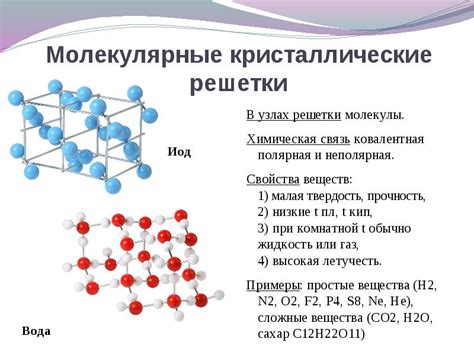
Примеры молекулярных веществ:
- Вода (H2O) – состоит из молекул, состоящих из атомов водорода и кислорода.
- Метан (CH4) – состоит из молекул, состоящих из атомов углерода и водорода.
- Сахар (C12H22O11) – состоит из молекул, состоящих из атомов углерода, водорода и кислорода.
Немолекулярные вещества – это вещества, состоящие не из молекул, а из отдельных атомов или ионов, связанных между собой электростатическими силами. Немолекулярные вещества обычно обладают высокой температурой кипения и плавления и не имеют определенной молекулярной структуры.
Примеры немолекулярных веществ:
- Натрий (Na) – вещество, состоящее из отдельных атомов натрия.
- Хлор (Cl2) – вещество, состоящее из молекул, состоящих из двух атомов хлора.
- Железо (Fe) – вещество, состоящее из отдельных атомов железа.
Таким образом, основное отличие между молекулярными и немолекулярными веществами заключается в их структуре и типе связей между атомами или молекулами.
Важность понимания различий между веществами молекулярного и немолекулярного строения
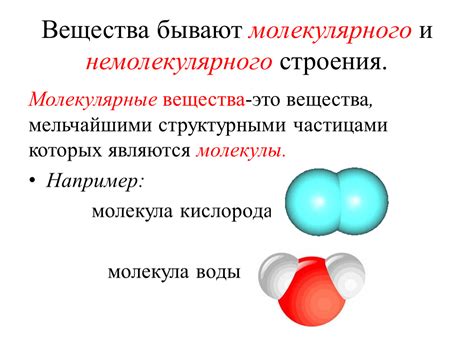
Вещества молекулярного строения состоят из молекул, которые образуются путем химического соединения атомов. Молекулы могут быть сложными и содержать различные элементы. Примерами веществ молекулярного строения являются вода, метан, аммиак и многие органические соединения. Основное свойство таких веществ - их относительная независимость молекул друг от друга. Благодаря этому свойству вещества молекулярного строения имеют низкую плотность и они обычно находятся в газообразном или жидком состоянии.
Вещества немолекулярного строения, наоборот, состоят из отдельных атомов или ионов, которые образуют регулярную кристаллическую структуру. Примерами таких веществ являются соли, металлы и большинство неорганических соединений. Основное свойство веществ немолекулярного строения - их высокая упорядоченность и взаимодействие между атомами или ионами. Благодаря этим свойствам вещества немолекулярного строения обладают высокой плотностью и обычно находятся в твердом состоянии.
Понимание различий между веществами молекулярного и немолекулярного строения имеет важное значение в различных областях. В химической индустрии, например, это понимание позволяет разрабатывать новые материалы и соединения, а также предсказывать и объяснять их свойства и взаимодействия. В фармацевтике понимание молекулярного строения веществ позволяет разрабатывать новые лекарственные препараты с нужными свойствами. В материаловедении понимание немолекулярного строения веществ помогает создавать новые материалы с уникальными свойствами и использовать их в различных областях, таких как электроника и энергетика.
В общем, понимание различий между веществами молекулярного и немолекулярного строения играет критическую роль в различных научных, технических и промышленных сферах и позволяет разрабатывать новые материалы, лекарства и технологии для решения различных задач.



