Свежеосажденный гидроксид меди 2 является одним из наиболее интересных и важных соединений меди. Он обладает рядом уникальных свойств, которые делают его полезным для различных применений в различных областях науки и техники.
Один из основных характеристических свойств свежеосажденного гидроксида меди 2 - его высокая активность. Это позволяет ему легко реагировать с различными веществами и становиться ключевым компонентом во множестве химических процессов и синтезов. Кроме того, его активность также обеспечивает ему хорошую растворимость в воде и других растворителях, что делает его удобным для работы в жидком состоянии.
Важно отметить, что свежеосажденный гидроксид меди 2 также обладает необычными оптическими свойствами. Благодаря своей структуре и электронной конфигурации, он способен пропускать определенный спектр видимого света, что делает его интересным материалом для применения в оптических устройствах и приборах.
Кроме того, свежеосажденный гидроксид меди 2 обладает и другими химическими реакциями и свойствами, которые находят применение в различных областях науки и промышленности. Например, его способность к адсорбции различных веществ делает его полезным в качестве катализатора в химических реакциях. Также его высокая термическая стабильность позволяет использовать его в высокотемпературных процессах.
Свойства свежеосажденного гидроксида меди 2

Получение данного вещества происходит путем осаждения ионов меди 2 из водных растворов с соответствующими осадителями, например, натриевым или аммиачным гидроксидами.
Главные свойства свежеосажденного гидроксида меди 2:
- Аморфная структура. Гидроксид меди 2 обладает безструктурной кристаллической решеткой, что придает веществу определенные свойства, такие как высокая реакционная активность и способность к изменению своей формы.
- Растворимость в воде. Гидроксид меди 2 хорошо растворяется в воде, образуя гидроксокомплексы, которые играют важную роль в многих биохимических и физико-химических процессах.
- Щелочные свойства. Гидроксид меди 2 проявляет щелочные свойства, способность образовывать гидроксокомплексы и взаимодействовать с кислотами.
- Окислительные свойства. Гидроксид меди 2 может служить окислителем в различных химических реакциях, например, с восстановлением некоторых органических соединений.
- Фоточувствительность. Гидроксид меди 2 обладает способностью поглощать световую энергию и использовать ее для проведения различных фотохимических реакций.
Таким образом, свежеосажденный гидроксид меди 2 является важным объектом исследования в химии и имеет широкий спектр свойств и возможностей.
Физические свойства
Этот соединение образует амфотерные растворы, то есть способен проявлять как свойства кислоты, так и свойства щелочи. Это значит, что гидроксид меди 2 может реагировать как с кислотными, так и с основными соединениями, образуя с ними соли.
Одно из уникальных свойств гидроксида меди 2 – его способность образовывать гидраты. Гидрат – это соединение, в котором молекулы воды связаны с молекулами гидроксида меди 2. Гидраты гидроксида меди 2 имеют разные степени гидратации, что влияет на их физические и химические свойства.
Из-за высокой токсичности гидроксида меди 2, при работе с ним следует соблюдать осторожность и использовать защитную экипировку, чтобы избежать попадания вещества на кожу и слизистые оболочки.
Химические свойства

1. Окислительное действие: Гидроксид меди 2 способен проявлять окислительное действие при взаимодействии с различными веществами. Он активно взаимодействует с органическими соединениями, давая возможность проводить реакции окисления и получения новых продуктов.
2. Реакция со соляной кислотой: При добавлении гидроксида меди 2 к соляной кислоте происходит реакция образования гидроксида меди 2. Реакция сопровождается выделением газа и образованием воды.
3. Растворимость в воде: Гидроксид меди 2 обладает ограниченной растворимостью в воде. При добавлении его в воду происходит образование гидроксида и гидратированных ионов меди 2. При этом раствор приобретает голубоватый оттенок.
4. Взаимодействие с аммиаком: Гидроксид меди 2 активно взаимодействует с аммиаком, образуя сложные ионы. Под воздействием аммиака гидроксид меди 2 растворяется, образуя синий раствор с аммиаком.
5. Образование осадка: При взаимодействии гидроксида меди 2 с растворами солей кислот происходит образование осадка – гидроксида меди 2. Осадок имеет характерный голубой цвет и химическую формулу Cu(OH)2.
Таким образом, свежеосажденный гидроксид меди 2 проявляет ряд химических свойств, которые делают его важным соединением в различных промышленных и научных областях.
Реакции с водой

Свежеосажденный гидроксид меди 2 обладает высокой активностью в отношении воды. При взаимодействии с водой образуется раствор с голубым оттенком и молекулами воды происходят следующие химические реакции:
- Протолиз: гидроксид меди 2 образует ион гидроксида Cu(OH)2- и положительные ионы меди Cu2+. Эта реакция происходит с выделением тепла и характеризуется ростом температуры раствора.
- Гидратация: ионы меди Cu2+ претерпевают гидратацию, образуя комплексные ионы Cu(H2O)62+. При этом происходит образование водорода H2, который выделяется в виде пузырьков.
Реакция с водой является одной из основных реакций, которые свежеосажденный гидроксид меди 2 может совершать. Взаимодействие с водой приводит к образованию специфических соединений и изменению цвета раствора, что является важным фактором при использовании его в различных химических исследованиях.
Реакции с кислотами
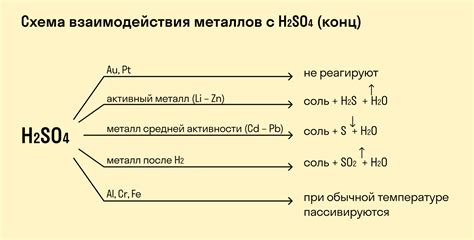
Свежеосажденный гидроксид меди 2 проявляет реактивность при контакте с кислотами.
Когда свежеосажденный гидроксид меди 2 вступает в реакцию с кислотами, происходит образование солей меди 2 и воды. Например, при взаимодействии с соляной кислотой, образуется хлорид меди 2:
Cu(OH)2 + 2HCl → CuCl2 + 2H2O
Аналогично, при реакции с нитратной кислотой образуется нитрат меди 2:
Cu(OH)2 + 2HNO3 → Cu(NO3)2 + 2H2O
Свежеосажденный гидроксид меди 2 также реагирует с карбонатной кислотой, образуя карбонат меди 2:
Cu(OH)2 + H2CO3 → CuCO3 + 2H2O
Реакции с кислотами позволяют использовать свежеосажденный гидроксид меди 2 как компонент при получении различных медных солей и продуктов химических реакций.
Взаимодействие с основаниями

Гидроксид меди 2 обладает щелочными свойствами и активно взаимодействует с основаниями. При этом происходит образование соответствующих солей меди 2 и воды.
Примером такого взаимодействия может служить реакция между гидроксидом меди 2 и гидрооксидом натрия (NaOH). В результате образуется медианатриевая соль (CuNaO2) и вода.
Cu(OH)2 + 2NaOH → CuNaO2 + 2H2O
Взаимодействие гидроксида меди 2 с основаниями основывается на образовании связи между одним атомом меди и одним атомом основания через кислородный атом. В результате такой связи образуется ионная соль, которая растворяется в воде, а также вода как побочный продукт реакции.
Термическое разложение
Cu(OH)2 → CuO + H2O
Этот процесс протекает при температуре около 250-300 градусов Цельсия. Термическое разложение гидроксида меди 2 приводит к изменению его физических и химических свойств.
Полученный оксид меди (II) обладает важными свойствами, которые делают его полезным в различных процессах и реакциях. Он является твердым веществом, имеющим черный или коричневый цвет. Кроме того, оксид меди (II) обладает полупроводниковыми свойствами и может использоваться, например, в производстве полупроводниковых приборов.
Термическое разложение гидроксида меди 2 является важным этапом для понимания его химической природы и возможностей применения в различных областях науки и технологии.
Реакции с оксидами

При соприкосновении с оксидами, гидроксид меди 2 проявляет амфотерные свойства, то есть может проявлять как кислотные, так и основные свойства. При этом реакции могут протекать с образованием солей или комплексных соединений.
Например, гидроксид меди 2 может реагировать с оксидом алюминия, Al2O3, и образовывать соль – медь(II)алюминат:
Al2O3 + 3Cu(OH)2 → 2CuAlO2 + 6H2O
Также гидроксид меди 2 может взаимодействовать с оксидом железа(III), Fe2O3, и образовывать медь(II)феррат:
Fe2O3 + 3Cu(OH)2 → 2CuFeO2 + 3H2O
Такие реакции позволяют использовать гидроксид меди 2 для получения различных соединений и материалов.
Применение

Свежеосажденный гидроксид меди 2 обладает широким спектром применения в различных отраслях:
- Химическая промышленность:
- Производство красителей и пигментов;
- Изготовление электродной проволоки;
- Получение индикаторов для оптической микроскопии;
- Использование в качестве катализатора в различных реакциях;
- Производство жидкостей для радиаторов.
- Электронная промышленность:
- Производство полупроводниковых элементов и интегральных схем;
- Изготовление проводящих пленок и покрытий;
- Применение в составе фоточувствительных пленок.
- Медицина:
- Использование в качестве антисептика и дезинфицирующего средства;
- Производство медицинских препаратов;
- Использование в составе эмбриодермальных мазей;
- Применение в стоматологии для обработки корневых каналов.
- Строительство и отделка:
- Использование при производстве керамической и глазурованной плитки;
- Применение в составе строительных растворов и штукатурок;
- Получение декоративных покрытий и фасадов.
- Производство бумаги и текстиля:
- Применение в качестве катионного активатора при получении целлюлозы и бумаги;
- Использование в процессе окрашивания тканей и волокон.
Также свежеосажденный гидроксид меди 2 может использоваться в лабораторных исследованиях, в качестве компонента косметических средств, антифризов и других продуктов повседневного использования.



