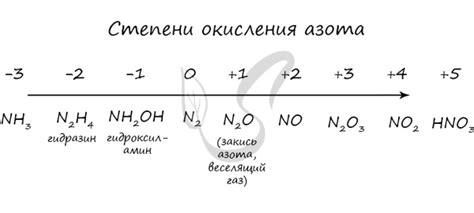
Азот - химический элемент из группы пневматических, он встречается в природе в различных соединениях. Степень окисления азота в этих соединениях имеет огромное значение для понимания его химических свойств и реакций. Степень окисления азота является одной из важнейших характеристик его химической активности.
Степень окисления азота в соединениях может быть положительной (показвается числом со знаком "+") или отрицательной (показывается числом со знаком "-"). Она указывает на количество электронов, которые азот принимает или отдает при образовании химических связей. Положительная степень окисления означает, что азот отдает электроны и приобретает положительный заряд, а отрицательная - что азот принимает электроны и приобретает отрицательный заряд.
Степень окисления азота в соединениях зависит от других элементов, с которыми он образует химические связи. Например, в соединениях с кислородом (оксид азота) азот имеет степень окисления +2, +4 и +5. В соединениях с водородом (амины) степень окисления азота может быть -3. В соединениях с металлами азот обычно имеет степень окисления -3, -2 или -1. Таким образом, степень окисления азота в соединениях является важным индикатором его свойств и реактивности.
Типы соединений азота
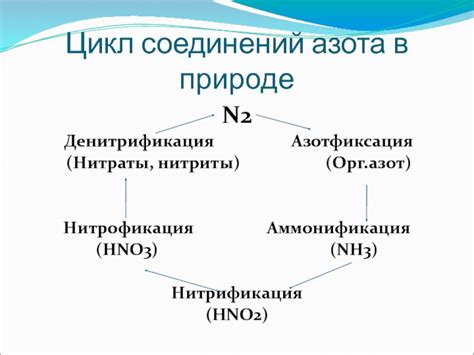
Один из наиболее распространенных типов соединений, содержащих азот, - это азотистые основания. Они образуются при сочетании азота с элементами 1-й группы, такими как литий, натрий, калий. Примером может служить гидроксид аммония (NH4OH), который получается при растворении аммиака (NH3) в воде.
Другой тип соединений азота - это азотистые основы, образованные при соединении азота с элементами 2-й группы, например, магнием, кальцием или барием. Сертификатами могут быть азотистые основы, такие как гидроксид амиды (Mg(NH2)2), которые содержат два атома азота, связанные с атомом металла и группой NH2.
Соединения азота также могут быть представлены нитратами (NO3-), нитритами (NO2-) и амидами (NH2-). Они образуются при сочетании азота с кислородом или серой и являются распространенными веществами в химической промышленности и ежедневной жизни.
Таким образом, азот способен образовывать различные типы соединений в зависимости от его валентности и природы окружающих атомов. Изучение свойств и реакционной способности этих соединений позволяет более полно понять химию азота и его взаимодействие с другими элементами.
Степень окисления азота в органических соединениях

Степень окисления азота в органических соединениях может быть различной, в зависимости от образующихся связей и групп функциональности.
В амминах и амидных соединениях азот обычно имеет степень окисления -3, поскольку атом азота образует три связи с водородом или углеродными атомами.
В нитро соединениях азот имеет степень окисления +3, поскольку образуется связь между азотом и оксигеном.
В нитрозах, оксимах и гидроксиламине азот имеет степень окисления +1, поскольку образуется связь между азотом и кислородом или водородом.
В нитратных соединениях азот имеет степень окисления +5, поскольку образуются связи между азотом и несколькими оксигенами.
Таким образом, степень окисления азота в органических соединениях может принимать значения от -3 до +5, что зависит от типа связей и групп функциональности, образованных азотом.
Степень окисления азота в неорганических соединениях

Азот может образовывать различные неорганические соединения, в которых его степень окисления может быть различной. Степень окисления азота показывает, сколько электронов азот "отдал" или "получил" в ходе образования соединения.
Степень окисления азота в неорганических соединениях может быть положительной, отрицательной или равной нулю.
Азот может иметь положительную степень окисления, когда он принимает на себя один или несколько электронов от других элементов. Например, в нитрате аммония (NH4NO3) азот имеет степень окисления +5, так как он принял пять электронов от кислорода.
Азот может иметь отрицательную степень окисления, когда он отдает один или несколько электронов другим элементам. Например, в азиде натрия (NaN3) азот имеет степень окисления -3, так как он отдал три электрона натрию.
Азот также может иметь степень окисления, равную нулю, когда он находится в элементарном состоянии или во многих органических соединениях. Например, в азоте (N2) и аммиаке (NH3) степень окисления азота равна нулю.
Важно помнить, что степень окисления азота может изменяться в зависимости от условий реакции и окружающей среды.
Практическое применение знания о степени окисления азота
Знание о степени окисления азота позволяет производителям точно расчеть состав исходных реагентов и определить необходимое количество реагентов для получения требуемых продуктов. Это особенно важно при производстве различных химических соединений, таких как азотные удобрения, кислоты и основания, аммиак, нитраты и многое другое. Знание о степени окисления азота позволяет контролировать стехиометрические пропорции реагентов и улучшить качество получаемой продукции.
Кроме того, знание о степени окисления азота позволяет ученым и исследователям в области биологии и экологии изучать и анализировать биогеохимические циклы азота в природе. Это помогает разработать стратегии по увеличению эффективности использования азотных удобрений, а также по снижению выбросов азотных соединений в окружающую среду, что способствует защите экологического равновесия и предотвращению загрязнения окружающей среды азотными соединениями.
Знание о степени окисления азота также находит применение в медицине и фармацевтике. Оно позволяет разрабатывать новые лекарственные препараты, основанные на азотсодержащих органических соединениях, таких как аминокислоты, нуклеотиды и другие молекулы, в которых азот играет важную роль. Знание о степени окисления азота также помогает ученым изучать и понимать особенности биохимических реакций, происходящих в живых организмах, и разрабатывать методы лечения различных заболеваний.
В целом, практическое применение знания о степени окисления азота позволяет улучшать процессы производства, защищать окружающую среду от загрязнения, разрабатывать новые лекарственные препараты и углублять наше понимание о жизни и ее процессах. Поэтому изучение степени окисления азота является важной частью образования в области химии и имеет большую практическую ценность.



