Вещества – это все то, что нас окружает. Они состоят из маленьких частиц, называемых атомами. Атомы объединяются в молекулы, которые в свою очередь могут образовывать соединения.
Основные элементы, из которых состоят все вещества, известны с древних времен. Всего известно около 120 химических элементов. Наиболее известными из них являются железо, серебро, золото, углерод и кислород.
У каждого элемента есть свои уникальные свойства. Например, золото – это блестящий металл желтого цвета. Серебро имеет блестящую поверхность и проводит ток, а углерод – это черный твердый материал, из которого изготавливают карандаши.
Изучение химических элементов и их свойств помогает нам понять, как устроен мир вокруг нас. Это интересное и важное направление в науке, которое помогает разгадывать все новые тайны природы и разрабатывать новые материалы и технологии.
Состав и свойства веществ. 7 класс. Основные элементы.
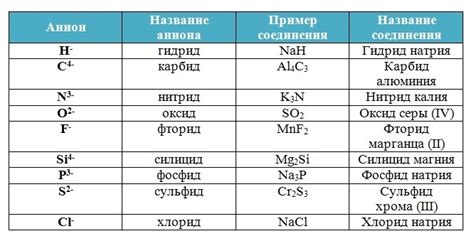
Каждому основному элементу соответствует символ - это знак или буква, которым обозначается элемент. Например, гидроген - H, углерод - С, кислород - О.
Основные элементы имеют свои уникальные свойства. Некоторые из них являются металлами, другие - неметаллами, и есть также элементы, которые находятся между металлами и неметаллами и называются полуметаллами.
- Металлы обладают блеском, хорошей проводимостью электричества и тепла, а также высокой пластичностью и твердостью.
- Неметаллы обычно обладают неблагородными свойствами, такими как непроводимость электричества и тепла, хрупкость и низкая твердость.
- Полуметаллы обладают промежуточными свойствами между металлами и неметаллами.
Кроме того, основные элементы имеют определенную атомную массу, которая показывает, сколько атомов вещества содержится в одной молекуле.
Знание основных элементов и их свойств является важным для понимания химических реакций и состава веществ, а также для дальнейшего изучения химии и других естественных наук.
Два вида веществ

Элементы – это типы веществ, которые не могут быть разделены на более простые вещества. Например, кислород, углерод, железо и алюминий являются элементами. Каждый элемент имеет свою химическую символику, например, кислород обозначается символом "O", а углерод – "C".
Соединения – это вещества, которые образуются путем соединения двух или более элементов. В отличие от элементов, соединения могут быть разложены на более простые вещества. Например, вода – это соединение водорода и кислорода, обозначается символом "H2O". Соединения могут иметь новые свойства, которые отличаются от свойств элементов, из которых они образованы.
Все элементы и соединения имеют свои уникальные свойства, которые определяют, как они взаимодействуют с другими веществами. Понимание этих свойств позволяет ученым и инженерам создавать новые материалы и улучшать уже существующие.
Простые и сложные вещества
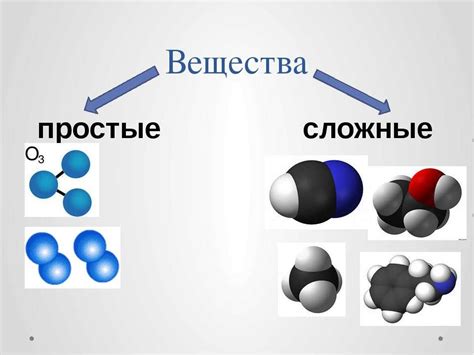
Простые вещества представлены одним типом атомов, которые не могут быть разложены на более простые вещества химическими методами. Примерами простых веществ могут служить химические элементы, такие как кислород (O), водород (H), углерод (C) и многие другие. Основные свойства простых веществ определяются их атомными структурами и электронной конфигурацией.
С другой стороны, сложные вещества состоят из двух или более различных элементов, объединенных химическими связями. Они могут быть разложены на простые вещества химическими реакциями. Примерами сложных веществ могут служить вода (H2O), соль (NaCl), молекулы углеводородов и другие. Сложные вещества имеют уникальные химические свойства, определяющие их поведение в различных химических реакциях и взаимодействие с другими веществами.
Знание о простых и сложных веществах является основой для понимания основных принципов химии и рассмотрения различных химических процессов, происходящих в природе и в химической промышленности.
Основные элементы вещества

Каждый химический элемент имеет свои уникальные свойства, которые определяют его поведение в химических реакциях. Некоторые элементы хорошо проводят ток, их называют металлами. Примеры таких элементов: железо, медь, алюминий. Другие элементы не проводят ток и обладают хрупкостью, их называют неметаллами. Примеры таких элементов: кислород, углерод, сера.
Также существует группа элементов, которые обладают свойствами и металлов, и неметаллов. Их называют полуметаллами или металлоидами. Примеры таких элементов: кремний, германий, мышьяк.
Каждый элемент имеет свой уникальный химический символ, который указывается на периодической системе. Например, углерод обозначается символом "С", железо - "Fe", сера - "S".
Основные элементы вещества играют важную роль в нашей жизни. Благодаря их свойствам мы можем создавать различные материалы, проводить электричество, готовить пищу и многое другое. Понимание основных элементов помогает ученым разрабатывать новые материалы и технологии.
Символы и свойства элементов
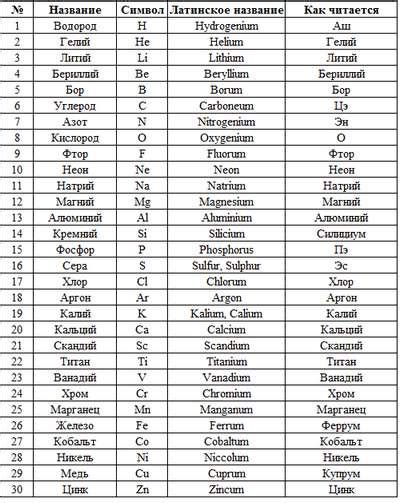
Символ элемента – это обозначение, состоящее из одной или двух букв латинского алфавита. Этот символ уникален для каждого элемента и помогает идентифицировать его в таблице химических элементов.
Кроме символов, каждый элемент имеет свои специфические свойства. Один из основных параметров в химии – атомная масса элемента. Она указывает на массу одного атома данного элемента в атомных единицах.
Еще одним важным свойством элемента является его относительная атомная масса. Она показывает, сколько раз атом данного элемента тяжелее атома водорода, которому присвоена масса 1 единица.
Атомный радиус – это еще одно свойство элемента. Он указывает на размер атома данного элемента и измеряется в пикометрах (пм).
Также элементы имеют свои электроотрицательности. Электроотрицательность отражает способность атома притягивать к себе электроны. Этот параметр важен при изучении химических связей и положения элемента в периодической системе.
Примеры элементов и их свойства:
- Углерод (C) – атомная масса: 12,01, относительная атомная масса: 12, атомный радиус: 77 пм, электроотрицательность: 2,55.
- Кислород (O) – атомная масса: 16,00, относительная атомная масса: 16, атомный радиус: 73 пм, электроотрицательность: 3,44.
- Натрий (Na) – атомная масса: 22,99, относительная атомная масса: 23, атомный радиус: 186 пм, электроотрицательность: 0,93.
Знание символов и свойств элементов помогает химикам понимать и выявлять закономерности в строении веществ и их химическом поведении.
Химические связи в веществах
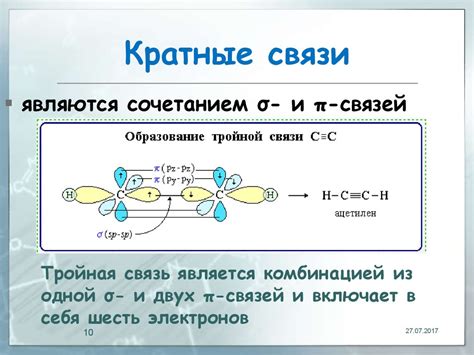
Все вещества состоят из атомов, которые могут связываться друг с другом, образуя химические связи. Химические связи определяют свойства вещества и его структуру.
Существуют три основных типа химических связей:
- Ионные связи. Ионные связи образуются между атомами с разным электрическим зарядом. Атомы с положительным зарядом (катионы) и атомы с отрицательным зарядом (анионы) притягиваются друг к другу и образуют ионные соединения. Примерами ионных соединений являются хлорид натрия (NaCl) и гидроксид калия (KOH).
- Ковалентные связи. Ковалентные связи образуются, когда атомы делят электроны, чтобы достичь стабильной электронной конфигурации. В ковалентных связях электроны общие и могут быть расположены между атомами или парой атомов. Примерами веществ с ковалентными связями являются молекулы воды (H2O) и метана (CH4).
- Металлические связи. Металлические связи характерны для металлов. В этом типе связи атомы металла образуют решетку, где их валентные электроны свободно движутся между атомами и образуют общую электронную оболочку. Эти электроны могут легко передвигаться, создавая проводимость вещества. Примерами металлических связей являются железо (Fe), алюминий (Al) и медь (Cu).
Химические связи между атомами определяют не только физические и химические свойства вещества, но и его реакционную способность.
Основные свойства вещества
Все вещества обладают определенными свойствами, которые позволяют их идентифицировать и характеризовать. Некоторые из основных свойств вещества включают:
- Масса: каждое вещество имеет массу, которая определяется количеством вещества в нем. Масса измеряется в граммах или килограммах.
- Объем: объем вещества указывает на пространство, занимаемое этим веществом. Объем измеряется в литрах или кубических сантиметрах.
- Плотность: это отношение массы вещества к его объему. Плотность является характеристикой материала и измеряется в граммах на кубический сантиметр или килограммах на литр.
- Точка плавления: точка плавления - это температура, при которой вещество переходит из твердого состояния в жидкое состояние.
- Точка кипения: точка кипения - это температура, при которой вещество переходит из жидкого состояния в газообразное состояние.
- Растворимость: растворимость указывает на способность вещества растворяться в другом веществе. Вещество может быть полностью растворимым, нерастворимым или частично растворимым.
- Химические свойства: вещества обладают химическими свойствами, которые определяют, как они реагируют с другими веществами. Эти свойства могут включать горение, окисление или окрашивание.
Знание основных свойств вещества позволяет нам лучше понять его поведение, взаимодействие с другими веществами и применение в различных областях науки и промышленности.



