Разбавленная серная кислота, часто называемая сульфатной кислотой, является одним из наиболее распространенных и опасных химических веществ в промышленности. Она является сильным окислителем и может вызвать серьезные ожоги на коже и слизистых оболочках, если попадет на них. Поэтому важно знать, какие вещества могут нейтрализовать разбавленную серную кислоту, чтобы минимизировать ее воздействие на организм.
Одним из эффективных способов нейтрализации разбавленной серной кислоты является использование щелочей, таких как гидроксиды натрия (NaOH) или калия (KOH). Эти вещества обладают высокой щелочной активностью и могут превратить серную кислоту в нейтральные соли, что делает ее менее опасной для окружающей среды и тела человека. Однако при работе с гидроксидами необходимо быть осторожными, так как они сами являются жесткими щелочами и также могут вызывать ожоги.
Кроме того, для нейтрализации разбавленной серной кислоты можно использовать щелочные растворы, содержащие карбонаты, бикарбонаты и гидрокарбонаты натрия или калия. Эти соединения обладают щелочной активностью и также способны нейтрализовать серную кислоту, образуя соли и углекислый газ. Они менее опасны для работы, чем гидроксиды, но все равно требуют соблюдения мер предосторожности.
Как справиться с разбавленной серной кислотой
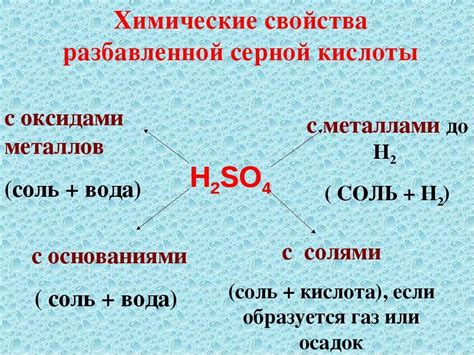
Перед тем как приступить к нейтрализации разбавленной серной кислоты, необходимо принять соответствующие меры безопасности. Это включает ношение защитной одежды, резиновых перчаток и очков, а также обеспечение хорошей вентиляции помещения.
Самым эффективным способом нейтрализации разбавленной серной кислоты является использование раствора щелочи, такой как гидроксид натрия (NaOH) или гидроксид кальция (Ca(OH)2). Это происходит в результате реакции с образованием соли и воды, что позволяет безопасно устранить кислотное вещество.
| Щелочь | Реакция нейтрализации |
|---|---|
| Гидроксид натрия (NaOH) | H2SO4 + 2NaOH -> Na2SO4 + 2H2O |
| Гидроксид кальция (Ca(OH)2) | H2SO4 + Ca(OH)2 -> CaSO4 + 2H2O |
При нейтрализации серной кислоты необходимо следовать определенным шагам:
- Осторожно налить щелочь в разбавленную серную кислоту, избегая брызг и попадания кислоты на кожу или одежду. Заметьте, что реакция будет сопровождаться выделением тепла.
- Тщательно перемешивать смесь до тех пор, пока нейтрализация не будет полностью завершена. Она будет сопровождаться изменением цвета смеси и прекращением выделения газов.
- После завершения реакции собрать остатки смеси в непроницаемую емкость для дальнейшей бережной утилизации.
- Очистить место работы и инструменты от остатков кислоты и щелочи, используя воду и нейтрализующие вещества, такие как карбонат натрия (Na2CO3) или гидрокарбонат натрия (NaHCO3).
Важно помнить, что нейтрализация разбавленной серной кислоты должна осуществляться только под контролем профессионалов, так как неправильное выполнение данных действий может быть опасно для окружающей среды и человеческого здоровья.
Предопределенные вещества

Существует несколько предопределенных веществ, которые могут использоваться для нейтрализации разбавленной серной кислоты, так как эти вещества обладают свойствами, противодействующими ее кислотности. Некоторые из них включают:
- Гидроксид натрия: Это щелочное вещество, которое реагирует с серной кислотой, образуя соль и воду.
- Гидроксид калия: Аналогично гидроксиду натрия, гидроксид калия также реагирует с серной кислотой, образуя соль и воду.
- Углекислый газ: Для нейтрализации разбавленной серной кислоты углекислым газом может использоваться реакция с добавлением газа в воду, что приведет к образованию угольной кислоты.
- Карбонат натрия: Этот сольный сернокислый натрий, который также может нейтрализовать разбавленную серную кислоту.
Выбор определенного вещества для нейтрализации может зависеть от конкретной ситуации и требований. Важно учитывать совместимость и безопасность при использовании данных веществ.
Нейтрализация раствора с помощью щелочей
Разбавленная серная кислота (H2SO4) является одной из наиболее распространенных кислот в промышленных процессах и лабораторных исследованиях. Когда этот раствор соприкасается с щелочами, такими как натриевая гидроксид (NaOH) или калиевая гидроксид (KOH), они реагируют между собой, образуя соль и воду:
- Щелочь (NaOH или KOH) растворяется в воде, образуя ионы гидроксидов (OH-)
- Ионы гидроксидов реагируют с ионами водорода (H+) в разбавленной серной кислоте, образуя воду (H2O)
- Оставшиеся ионы соединяются, образуя соль (например, Na2SO4 или K2SO4)
Таким образом, нейтрализация разбавленной серной кислоты с помощью щелочей приводит к образованию соли, которая является более безопасным и менее едким веществом, чем сама кислота.
Процесс нейтрализации раствора с помощью щелочей может быть использован для регулирования pH-значения в различных процессах и приложениях, таких как обработка сточных вод, производство удобрений и фармацевтическая промышленность.
Безопасность и рекомендации
Работа с разбавленной серной кислотой требует соблюдения определенных мер безопасности. Всегда носите защитную экипировку, включая защитные очки, резиновые перчатки и халат. При работе с разбавленной серной кислотой рекомендуется быть в хорошо проветриваемом помещении или использовать вытяжные системы для удаления паров.
В случае контакта разбавленной серной кислоты с кожей или глазами, немедленно промойте затронутое место большим количеством воды в течение 15 минут и обратитесь за медицинской помощью.
Не смешивайте разбавленную серную кислоту с другими химическими веществами без необходимости и не используйте металлическую посуду или инструменты при работе с ней. При хранении разбавленной серной кислоты следует использовать контейнеры из не реагирующего с ней материала, такого как полиэтилен или стекло.
Важно помнить, что разбавленная серная кислота может вызвать ожоги и другие травмы при неправильном обращении с ней. Поэтому рекомендуется тщательно изучить инструкции по использованию перед началом работы, следовать рекомендациям и обращаться за профессиональной консультацией при необходимости.



