Металлы и неметаллы – это две категории химических элементов, которые обладают разными свойствами и способностями. Когда происходит их соединение, возникают новые химические соединения, которые могут иметь совершенно различные свойства. В данной статье мы рассмотрим, что происходит на уровне атомов и молекул при соединении металлов и неметаллов.
Металлы обладают такими свойствами, как блеск, хорошая теплопроводность и электропроводность, высокая пластичность и деформируемость. Они имеют малую электроотрицательность и обычно образуют ионные соединения. С другой стороны, неметаллы имеют более высокую электроотрицательность и могут образовывать ковалентные соединения.
При соединении металлов и неметаллов происходит передача электронов от металла к неметаллу. Металл отдает одно или несколько электронов, становясь положительно заряженным ионом, а неметалл принимает эти электроны, становясь отрицательно заряженным ионом. Таким образом, возникает ионная связь, обуславливающая огромное количество химических соединений различной степени сложности.
Механизм соединения металла и неметалла
Соединение металла и неметалла осуществляется при взаимодействии их атомов или ионов. Этот процесс осуществляется на микроскопическом уровне и зависит от химических свойств взаимодействующих веществ.
- Ионные соединения: Металл отдает свои электроны неметаллу, образуя катион. Неметалл получает электроны и образует анион. Катионы и анионы притягиваются друг к другу силой электростатического притяжения, образуя кристаллическую решетку и ионное соединение.
- Ковалентные соединения: Атомы металла и неметалла обменивают электроны, чтобы достичь положения стабильной октетной оболочки. При этом образуются совместно используемые или связующие электроны. Между атомами образуется ковалентная связь, обеспечивающая силу притяжения и стабильность соединения.
- Металлические соединения: Атомы металла образуют решетку, в которой свободные электроны перемещаются между положительно заряженными атомами. Это создает так называемое "море свободных электронов" или "электронное облако", которое обеспечивает связь между атомами металла.
Механизм соединения металла и неметалла определяется их химическими свойствами и электронной структурой. Реакция соединения может происходить путем отдачи и приема электронов (ионное соединение), обмена электронами (ковалентное соединение) или перемещения свободных электронов (металлическое соединение).
Формирование ионообменных связей
При соединении металла и неметалла происходит формирование ионообменных связей. Ионы металла и неметалла образуют кристаллическую решетку, в которой ионы размещены в определенном порядке.
Формирование ионообменных связей происходит следующим образом:
| Металл | Неметалл |
|---|---|
| Отдает электроны | Принимает электроны |
| Образует положительные ионы | Образует отрицательные ионы |
| Ионы металла образуют катионную подрешетку | Ионы неметалла образуют анионную подрешетку |
| Катионы и анионы притягиваются друг к другу и образуют ионообменную связь | Связь основана на притяжении противоположно заряженных ионов |
Формирование ионообменных связей обуславливает химические и физические свойства соединения металла и неметалла. Ионообменные связи обладают высокой прочностью и способствуют образованию кристаллической структуры вещества. Кристаллическая решетка определяет многие свойства соединения, такие как твердотельная структура, плотность, температура плавления и т.д.
Влияние электроотрицательности на соединение
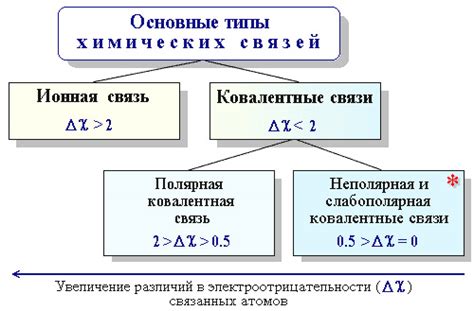
Если неметалл обладает более высокой электроотрицательностью, чем металл, происходит образование ионной связи. В этом случае, неметалл притягивает электроны, перенося их себе и образуя отрицательный ион, а металл становится положительным ионом. Получившиеся ионы притягиваются друг к другу, образуя кристаллическую решетку, что является основой ионного соединения.
Если разность электроотрицательностей между металлом и неметаллом невелика, образуется ковалентная связь. При этом электроны общие и перемещаются между атомами металла и неметалла, что позволяет им разделить некоторые электроотрицательности.
В обоих случаях, величина разности электроотрицательностей может определять силу и тип химической связи, а также физические свойства получившихся соединений. Более высокая электроотрицательность неметалла может привести к более поларной связи и, как результат, к более высоким температурам плавления и кипения, а также к лучшей растворимости в воде.
Влияние электроотрицательности на соединение является важным аспектом в химии и способствует пониманию связей и реакций между металлами и неметаллами.
Установление ковалентных связей
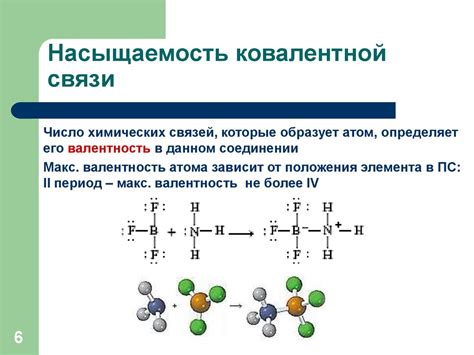
При соприкосновении металла и неметалла атомы обмениваются электронами таким образом, чтобы оба атома достигли наиболее стабильной энергетической конфигурации. Атом металла, у которого мало валентных электронов, отдает электрон(ы) атому неметалла с большим числом электронов в валентной оболочке. Такой обмен позволяет атомам обоих элементов достичь октетной конфигурации, когда в валентной оболочке находится 8 электронов.
Установление ковалентных связей между металлом и неметаллом позволяет создавать новые соединения с различными свойствами. Например, образование химических связей между металлом и неметаллом может привести к образованию соли или оксида, которые обладают разными физическими и химическими свойствами.
Ковалентная связь – важное явление в химии, она обеспечивает устойчивость различных соединений и определяет их свойства. Понимание процесса установления ковалентных связей между металлом и неметаллом имеет большое значение для практического использования и синтеза новых материалов с нужными свойствами.
Создание структуры кристаллической решетки
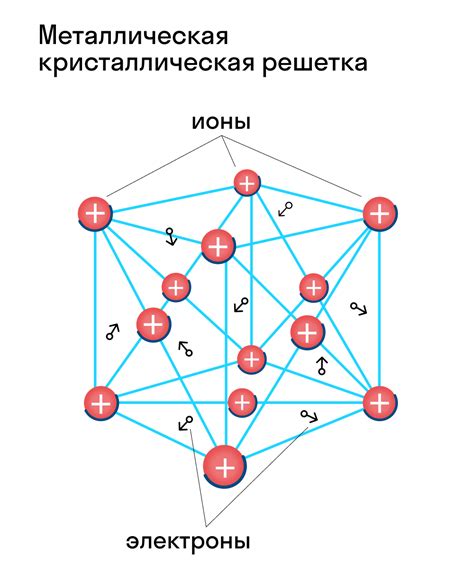
Когда металл соединяется с неметаллом, происходит образование кристаллической решетки, которая определяет основные свойства соединения. Структура решетки зависит от типа соединенных элементов и их атомной структуры.
В основе создания структуры кристаллической решетки лежит процесс обмена электронами между металлом и неметаллом. Когда металлический атом и неметаллический атом соединяются, происходит образование ионов и ионных связей.
Для примера, рассмотрим соединение натрия (Na) и хлора (Cl) для образования хлорида натрия (NaCl). Каждый атом натрия отдает свой внутренний электрон и образует положительный ион Na+, а каждый атом хлора принимает этот электрон и образует отрицательный ион Cl-. Получившиеся ионы притягиваются друг к другу и образуют кристаллическую решетку.
Структура решетки хлорида натрия обладает ионными связями, что делает ее структурным и электронным устройством устойчивым и мощным. В решетке каждый ион Na+ окружен шестью ионами Cl-, и каждый ион Cl- окружен шестью ионами Na+. Это создает регулярную трехмерную сетку и дает хлориду натрия устойчивую структуру.
Создание кристаллической решетки для других соединений между металлом и неметаллом происходит по схожим принципам, но структуры решеток могут отличаться в зависимости от типа атомной связи и атомных радиусов соединенных элементов.
Важной особенностью структуры кристаллической решетки является ее возможность обеспечивать электрическую проводимость, необходимую для многих металлов. Благодаря свободно перемещающимся электронам, металлы могут эффективно проводить электрический ток.
Формирование молекулярных соединений
Соединение металла и неметалла, приводящее к образованию молекулы, называется молекулярным соединением. В данном процессе происходит передача электронов от металла к неметаллу, что приводит к образованию ионов и связывению их в молекулу.
Для формирования молекулярных соединений металл и неметалл обычно образуют ковалентные связи. При этом электроны оболочек атомов металла и неметалла сопрягаются, образуя общие пары электронов, которые являются связью между атомами.
Формирование молекулярного соединения происходит при образовании структуры, в которой атомы металла и неметалла объединены в молекулу с помощью ковалентных связей. Количество и вид связей в молекуле зависит от степени окисления атомов, а также от их электронной конфигурации.
Молекулярные соединения имеют определенные физические и химические свойства, такие как температура плавления и кипения, растворимость в воде, реакционная способность и т. д. Эти свойства могут различаться в зависимости от типа молекулы и ее состава.
Молекулярные соединения широко применяются в различных областях науки и техники. Они играют важную роль в химической промышленности, фармацевтике, пищевой промышленности, электронике и других сферах. Изучение формирования молекулярных соединений помогает понимать их свойства и применение в практике.
Применение соединений металла и неметалла
Соединения металла и неметалла, такие как сплавы или керамика, имеют широкое применение в различных отраслях промышленности и науки.
Одним из наиболее распространенных применений таких соединений является производство материалов с улучшенными свойствами. Например, сплавы металлов с неметаллами могут обладать высокой прочностью и стойкостью к коррозии, что делает их идеальными для использования в строительстве, авиации и прочих отраслях, где требуются материалы с высокой надежностью и долговечностью.
Керамические материалы, состоящие из соединений металла и неметалла, используются в производстве посуды, изоляторов, керамической плитки и других изделий. Керамика обладает высокой стойкостью к высоким температурам, электрической изоляцией и химической устойчивостью, поэтому она широко применяется в промышленности и бытовых нуждах.
Соединения металла и неметалла также играют важную роль в электронике и электротехнике. Например, соединения полупроводников, таких как кремний, германий или галлий, используются в производстве полупроводниковых приборов, таких как транзисторы, микросхемы и светодиоды. Эти материалы обладают специфическими электрическими свойствами, делающими их основными компонентами современной электроники.
В области медицины соединения металла и неметалла применяются для создания стержней, пластин и имплантатов, используемых при ортопедических операциях и восстановительных процедурах. Эти материалы должны быть биосовместимыми, т.е. не вызывать отторжения организмом, и обладать достаточной прочностью для обеспечения долговременной поддержки и заживления тканей.
Таким образом, соединения металла и неметалла являются важными компонентами современных технологий и находят широкое применение в различных сферах человеческой деятельности.



