Азот (N2) – один из наиболее распространенных неметаллов в природе. Он также является важным элементом для многих живых организмов и широко используется в промышленности. Азот обладает уникальными свойствами, которые делают его незаменимым в различных сферах деятельности.
Один из основных химических характеристик азота – низкая растворимость в воде. Это свойство позволяет использовать его для создания защитной оболочки в окружающей среде, например в банках, содержащих пищевые продукты. Благодаря низкому содержанию кислорода, который может вызывать окисление, азот предотвращает разрушение продуктов и сохраняет их свежесть на протяжении длительного времени.
Кроме того, азот обладает еще одним важным неметаллическим свойством – низкой реактивностью. Это означает, что он не вступает в химическую реакцию с большинством других элементов, что делает его безопасным и стабильным в использовании. Например, азот часто используется как инертный газ в различных процессах, требующих отсутствия кислорода, чтобы предотвратить возможные взрывы или окисление веществ.
Уникальные свойства азота: химические особенности и проявления

1. Отсутствие окрашивания. Азот в своем чистом состоянии является безцветным газом. Это свойство позволяет использовать азот в различных областях промышленности, таких как производство электроники и пищевая промышленность, где цветозависимость может быть нежелательной.
2. Инертность. Азот является очень инертным газом и практически не взаимодействует с другими элементами. Это делает его незаменимым компонентом в пищевой и фармацевтической промышленности, где необходимо сохранять свежесть и стабильность продуктов.
3. Образование связей. Азот образует множество различных химических соединений, таких как аммиак, нитраты и азотные оксиды. Эти соединения имеют широкое применение в сельском хозяйстве, производстве удобрений и производстве взрывчатых веществ.
4. Превращение в синтезирующий газ. При достижении высоких температур и давления, азот может превращаться в синтезирующий газ, который затем используется в производстве азотной кислоты и других химических соединений.
5. Участие в биологических процессах. Азот играет важную роль в жизни организмов, так как является неотъемлемой частью аминокислот и нуклеиновых кислот, входящих в состав белков и ДНК соответственно.
Форма азота: газообразное состояние и его устойчивость
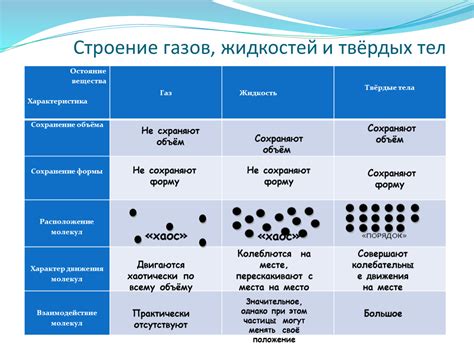
Азот представляет собой химический элемент, который находится в азотном состоянии в атмосфере Земли. В свободном состоянии азот представляет собой газовую форму, обладающую рядом особенностей и проявлений.
Газообразный азот обладает прозрачностью, отсутствием запаха и цвета. Он является неполярным и инертным газом, что делает его полезным при выполнении различных промышленных процессов и в химической промышленности.
Азот также характеризуется низкой плотностью и низкой теплопроводностью. Это позволяет ему использоваться в качестве изоляционного материала, например, в холодильной технике и вакуумных устройствах.
Газообразный азот обладает высокой устойчивостью и стабильностью при комнатной температуре и давлении. Он не поддерживает горение, поэтому может использоваться для предотвращения возгорания и взрывоопасных ситуаций. Благодаря своей стабильности азот также широко используется в пищевой и медицинской промышленности для сохранения свежести и предотвращения окисления продуктов.
Азотный цикл: роль в природных процессах и экологическая значимость
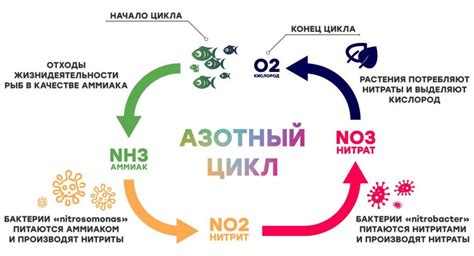
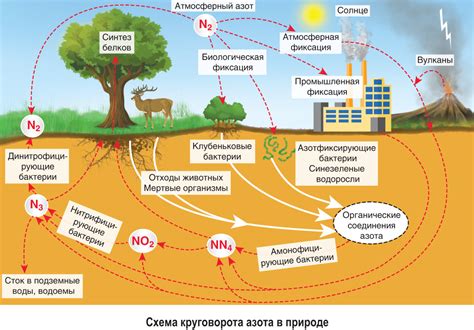
Азотный цикл представляет собой сложную систему взаимосвязанных процессов, где азот играет ключевую роль. Азотный цикл начинается с фиксации атмосферного азота, которая осуществляется некоторыми видами бактерий с помощью процессов азотфиксации. Полученный таким образом азот затем используется растениями для синтеза белка и других органических соединений.
После смерти растений и животных, азот из их остатков возвращается в почву в процессе азотификации, где опять же играют важную роль бактерии. Затем азот может быть выведен из почвы водой или попадать в грунтовые воды.
Азотный цикл также включает в себя процессы денитрификации, при которых азотные соединения превращаются в азот и попадают обратно в атмосферу. Это возможно благодаря щелочным условиям и наличию определенных бактерий.
Роль азотного цикла в природных процессах трудно переоценить. Азот является необходимым элементом для жизни всех организмов. Он является строительным материалом для белков, нуклеиновых кислот и многих других особо важных соединений. Без азота невозможно существование всех живых организмов на Земле.
Однако, через многие природные процессы азот попадает в водные системы и может вызывать значительные проблемы для экосистем. Избыток азота в водных системах может привести к размножению водорослей, что приводит к образованию плотных зеленых масс, которые мешают другим организмам получать достаточно света и кислорода.
Благодаря своей роли в природных процессах и экологической значимости азотный цикл является предметом изучения многих ученых. Понимание азотного цикла и его последствий позволяет нам принять меры для сохранения и восстановления экосистем и улучшения качества окружающей среды.
Азотные соединения: широкий спектр применений в промышленности

Азотные соединения, включающие азот в своей структуре, имеют огромное значение для промышленности и нашей повседневной жизни. Они обладают различными физическими и химическими свойствами, что позволяет использовать их в различных областях и процессах.
Одним из наиболее известных азотных соединений является аммиак (NH3). Аммиак широко используется в производстве удобрений, так как является важным источником азота для растений. Он также используется в производстве некоторых пластмасс, в качестве холодильного средства и при производстве чистящих средств.
Другим важным азотным соединением является нитрат натрия (NaNO3), который используется в производстве взрывчатых веществ и пиротехники. Нитрат натрия также является важным компонентом удобрений и используется в медицине.
Азотные оксиды, такие как оксид азота (NO) и диоксид азота (NO2), играют роль в формировании атмосферного азота, который является важным питательным элементом для растений. Они также используются в производстве кислот, красителей и пластмасс.
Карбамид (NH2CONH2), также известный как мочевина, является одним из основных азотных соединений, используемых в производстве удобрений. Он также используется в качестве компонента в косметических и медицинских препаратах, а также в производстве синтетических материалов.
Азид натрия (NaN3) используется в автомобильных подушках безопасности, так как при воздействии на него происходит экзотермическая реакция, обеспечивающая быстрое набухание подушки при аварии.
Это лишь некоторые примеры азотных соединений и их применений. Широкий спектр использования азотных соединений в промышленности подчеркивает их важность и значение в современном мире.
Биологическая роль азота: важность для растений и животных
У растений азот является неотъемлемым компонентом для синтеза белков, аминокислот и нуклеиновых кислот. Без азота растения не могут расти и развиваться правильным образом. Он необходим для образования хлорофилла, пигмента, который позволяет растениям поглощать солнечную энергию и осуществлять процесс фотосинтеза.
Азот также является ключевым элементом для животных. Он входит в состав белков, аминокислот, гормонов и нуклеиновых кислот. Белки, синтезируемые с использованием азота, являются строительными блоками тканей и органов животных. Аминокислоты, такие как глутамин, глицин и лейцин, играют важную роль в передаче нервных импульсов и образовании энергии.
Азот также участвует в образовании азотсодержащих соединений, таких как аммиак и нитраты, которые являются важными компонентами пищи для растений и животных. Растения поглощают нитраты и аммиак из почвы, используя их для роста и развития. Животные, в свою очередь, получают азот, потребный для своего организма, потребляя растительную и животную пищу.
Отсутствие азота может привести к различным проблемам в растениях и животных. Недостаток азота в почве может вызвать замедление роста растений, появление желтых и слабых листьев, а также низкую урожайность. У животных недостаток азота может привести к проблемам с пищеварением, иммунной системой и репродуктивными функциями.
- Азот играет важную роль в синтезе белков, аминокислот и нуклеиновых кислот.
- Азот является ключевым элементом для роста и развития растений.
- Азот входит в состав белков, аминокислот, гормонов и нуклеиновых кислот у животных.
- Азотсодержащие соединения являются важными компонентами пищи для растений и животных.
- Отсутствие азота может вызвать проблемы в росте и развитии организмов.
Взаимодействие азота с другими элементами: взрывоопасные смеси и реакции
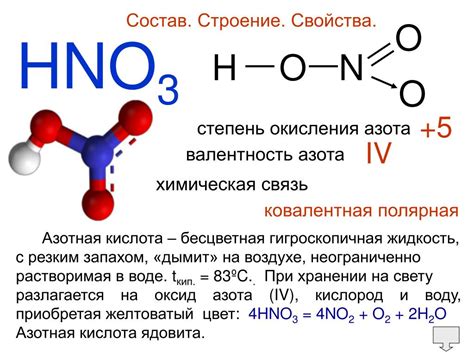
Один из наиболее распространенных примеров взаимодействия азота – образование аммиака (NH3) при реакции с водородом. Эта реакция может быть очень взрывоопасной при нарушении условий проведения и контроля. Аммиак используется в промышленности для производства удобрений, однако необходимо соблюдать все меры предосторожности и контролировать процесс образования и использования аммиака.
Азот также может взаимодействовать с кислородом, образуя оксид азота (NO) или оксиды азота более высокого порядка, такие как NO2 и N2O3. Оксиды азота являются вредными газами, которые могут вызывать различные заболевания дыхательной системы у людей и животных, а также наносить вред окружающей среде.
Реакция азота с металлами также может быть взрывоопасной. Например, при нагревании азот реагирует с медью, образуя пурпуровокрасное вещество, известное как медный азид (Cu3N2). Медный азид является взрывчатым соединением и может взрываться при механическом воздействии или при нагревании.
Взаимодействие азота с другими элементами требует аккуратности и контроля, особенно если речь идет о взрывоопасных смесях и соединениях. Предосторожные меры и технические регламенты должны быть соблюдены для обеспечения безопасности при работе с азотом и его соединениями.
Основные источники азота: природные и искусственные поставщики
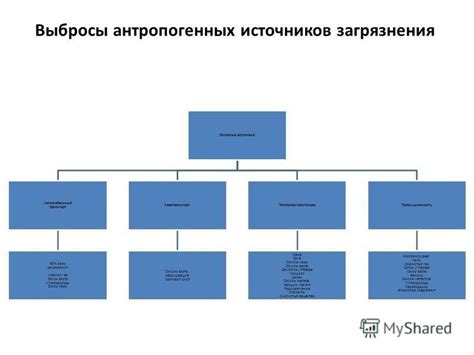
Основные природные источники азота включают:
- Атмосферный воздух: главным образом, азот получают растения с помощью процесса азотфиксации, выполняемого некоторыми видами бактерий.
- Почва: в почве азот существует в виде органических и неорганических соединений. Растения через корни поглощают неорганический азот в форме нитратов и аммония, а затем используют его для различных биологических процессов.
- Водные массы: азот присутствует в виде различных соединений в океанах, реках и озерах. Рыбы и другие водные организмы также используют азот для своего роста и развития.
Кроме природных источников, существуют и искусственные поставщики азота. Некоторые из них включают:
- Синтетическое производство азота: в промышленности широко используется процесс габаритного (теплового) разложения азота из воздуха для получения азотных удобрений и других химических соединений с азотом.
- Подкормки растений: для повышения урожайности и качества растений сельское хозяйство использует азотные удобрения, которые обогащают почву неорганическим азотом.
- Промышленные отходы: некоторые отрасли промышленности, такие как производство аммиака и нитратов, создают отходы, содержащие азот. Они могут быть использованы для производства азотных удобрений или подвергнуты переработке.
Источники азота играют важную роль в сельском хозяйстве, промышленности и экологических процессах. Умная и эффективная утилизация источников азота важна для обеспечения устойчивого развития и сохранения природных ресурсов.



