Нагревание жидкости - один из физических процессов, важных как для нашей повседневной жизни, так и для научных исследований. Когда мы нагреваем жидкость, происходит множество интересных явлений на молекулярном уровне.
Во-первых, при нагревании жидкости молекулы начинают двигаться быстрее. Это связано с увеличением их кинетической энергии. Молекулы получают энергию от нагревательного источника и начинают вибрировать и вращаться еще интенсивнее. Это делает жидкость более подвижной и изменяет ее физические свойства.
Во-вторых, при нагревании жидкости происходит испарение. Высокая температура приводит к возрастанию давления паров, что стимулирует переход жидкости в газообразное состояние. При этом молекулы покидают поверхность жидкости и переходят в газовую фазу. Этот процесс называется испарением и играет важную роль в таких явлениях, как кипение и конденсация.
Наконец, при нагревании жидкости может происходить денатурация белка. Высокая температура может изменить пространственную структуру белковых молекул, что приводит к потере их функциональности. Этот процесс наблюдается, например, при жарке яиц или при варке рыбы. Денатурация белка может изменить вкус, запах и текстуру продукта.
Влияние температуры на молекулы
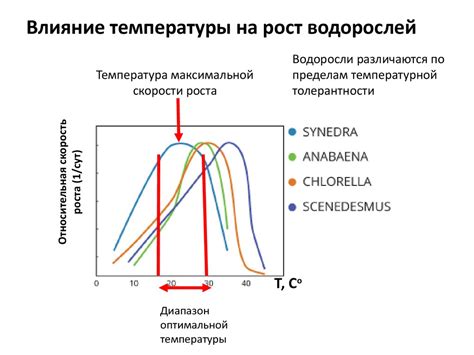
При нагревании жидкости молекулы получают энергию, что приводит к их возбуждению. В результате возбужденные молекулы начинают двигаться быстрее, увеличивая свое тепловое движение. Это приводит к увеличению расстояния между молекулами и растяжению связей между ними.
При достижении определенной температуры, называемой точкой кипения, молекулы становятся настолько энергичными, что начинают уходить из жидкости в виде пара. В этом состоянии молекулы уже не образуют взаимосвязанных структур и движутся независимо друг от друга.
Также повышение температуры может приводить к изменению фазы жидкости. Например, вода при нагревании до определенной температуры превращается в пар, а при охлаждении до определенной температуры превращается в лед. Это связано с изменением структуры и свойств молекул под воздействием тепловой энергии.
Таким образом, температура играет важную роль в изменении свойств и структуры молекул в жидкости. Повышение температуры приводит к увеличению энергии движения молекул, их возбуждению и изменению состояния жидкости.
Кинетическая энергия молекул
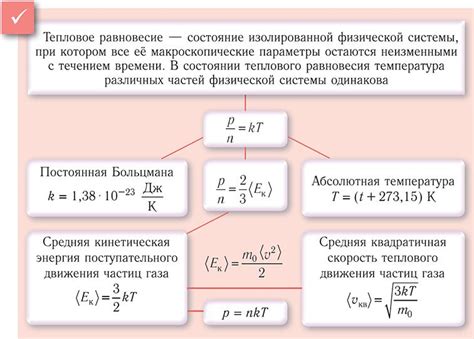
При нагревании жидкости молекулы начинают двигаться с большей скоростью, обладая кинетической энергией. Кинетическая энергия молекул пропорциональна их скорости и массе. Чем выше температура, тем больше кинетическая энергия молекул.
Увеличение кинетической энергии молекул ведёт к увеличению количества столкновений между ними. При столкновении молекулы могут передавать часть своей энергии друг другу, а также совершать взаимодействия с окружающими частицами.
Изменение кинетической энергии молекул при нагревании жидкости приводит к:
- Увеличению расстояния между молекулами и, как следствие, расширению жидкости.
- Усилению хаотичного движения молекул, что сказывается на вязкости жидкости.
- Более интенсивному испарению жидкости, так как молекулы приобретают достаточную энергию для преодоления силы притяжения и переходят в газообразное состояние.
Таким образом, кинетическая энергия молекул играет ключевую роль в процессах, связанных с нагреванием и изменением физических свойств жидкостей.
Изменение расстояний между молекулами
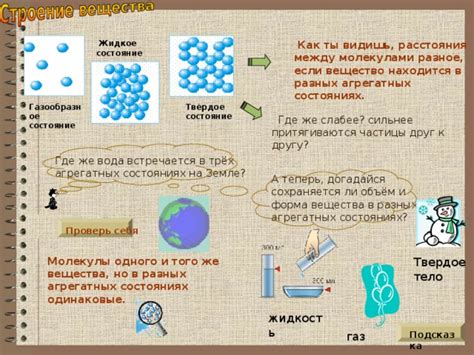
В жидкости молекулы держатся вместе силами межмолекулярных взаимодействий, таких как ван-дер-ваальсовы силы и водородные связи. При нагревании, кинетическая энергия молекул увеличивается, что приводит к возрастанию их движения. Молекулы начинают передвигаться, вращаться и колебаться с большей амплитудой.
В результате этого изменения, среднее расстояние между молекулами увеличивается. Расширение межмолекулярного расстояния приводит к увеличению объема жидкости. Изменение взаимного положения молекул оказывает влияние на различные свойства жидкости, такие как плотность, вязкость и теплопроводность.
Также, изменение расстояний между молекулами может приводить к изменению интермолекулярных сил, что в свою очередь влияет на фазовые переходы жидкости, например, на ее кипение или замерзание.
Изучение изменения расстояний между молекулами при нагревании жидкости позволяет понять механизмы, лежащие в основе изменения свойств и поведения жидкости в различных условиях.
Переход жидкости в газовую фазу

В начале процесса нагревания, молекулы вещества двигаются относительно медленно и находятся близко друг к другу. При нагревании происходит увеличение средней кинетической энергии молекул, что приводит к увеличению их скорости и отдалению друг от друга.
Когда средняя кинетическая энергия молекул превысит критическое значение, молекулы становятся достаточно энергичными, чтобы преодолеть притяжение других молекул и тем самым выйти из жидкого состояния. В этот момент начинается образование пара и происходит переход жидкости в газовую фазу.
Переход жидкости в газовую фазу сопровождается поглощением энергии, так как для перехода молекулы должны преодолеть силы притяжения. Эта энергия расходуется на преодоление сил воздействия притяжения молекул друг к другу, что приводит к эндотермическому процессу.
Процесс перехода жидкости в газовую фазу называется испарением. Испарение является важным процессом в природе и используется во многих технологических процессах, таких как сушка, дистилляция и кондиционирование воздуха.
Разрушение химических связей

При нагревании жидкостей происходит разрушение химических связей между атомами, что приводит к изменению свойств вещества. Разрушение химических связей может происходить различными путями в зависимости от типа вещества и условий нагревания.
Вода, например, состоит из атомов кислорода и водорода, связанных ковалентной связью. При нагревании жидкой воды энергия передается молекулам, и они начинают вибрировать с большей амплитудой. При достижении определенной температуры кинетическая энергия молекул становится достаточно большой, чтобы разорвать ковалентные связи между атомами. В результате образуется пар, состоящий из молекул воды, которые перемещаются в газообразное состояние.
Аналогичные процессы происходят и при нагревании других жидкостей. Молекулы начинают двигаться быстрее и вибрировать с большей амплитудой, что приводит к разрыву химических связей. В результате могут образовываться новые химические соединения или просто образуется газообразное состояние вещества.
Для некоторых веществ, таких как эфир или спирт, при нагревании происходит разрушение межмолекулярных сил притяжения, что приводит к возникновению пара этих веществ. В процессе нагревания эти вещества испаряются, образуют газы и покидают жидкость.
| Вещество | Процесс разрушения химических связей |
|---|---|
| Вода | Разрыв ковалентных связей между атомами кислорода и водорода |
| Эфир | Разрушение межмолекулярных сил притяжения |
| Спирт | Разрушение межмолекулярных сил притяжения |
В результате разрушения химических связей при нагревании жидкости происходят изменения физических и химических свойств вещества. Понимание этих процессов позволяет улучшить промышленные процессы, связанные с обработкой и использованием жидкостей в различных отраслях.
Образование новых соединений

При нагревании жидкости молекулы начинают двигаться с большей скоростью и частотой. Это приводит к возникновению новых физических и химических процессов, в результате которых образуются новые соединения.
Одним из типичных примеров образования новых соединений при нагревании жидкости является процесс эвполимеризации. Во время этого процесса две или более молекулы жидкости объединяются для образования большей молекулы, называемой полимером. Примером эвполимеризации является процесс, при котором молекулы этилена объединяются для образования полиэтилена - одного из самых распространенных пластиков.
Помимо эвполимеризации, при нагревании жидкостей могут происходить и другие химические процессы, такие как окисление или гидролиз. В результате этих процессов могут образовываться новые соединения с другими свойствами и структурой.
Важно отметить, что образование новых соединений при нагревании жидкости может быть как желательным, так и нежелательным явлением. Неконтролируемое образование новых соединений может приводить к разрушению или деградации жидкости, в то время как контролируемое образование новых соединений может использоваться в различных производственных процессах.
Изменение свойств жидкости
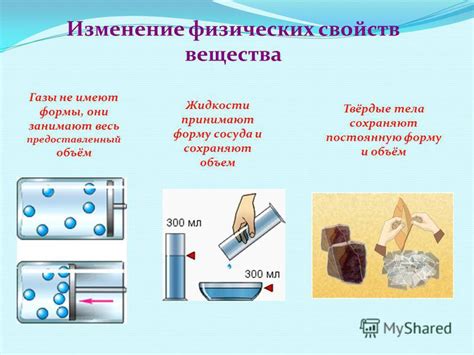
Нагревание жидкости приводит к изменению ее свойств. При повышении температуры молекулы жидкости получают больше энергии, увеличивается их кинетическая энергия и скорость движения. В результате молекулы начинают преодолевать силы внутреннего сцепления и разделяться, что приводит к увеличению объема жидкости.
Также при нагревании жидкости происходит расширение межмолекулярных расстояний и увеличение среднего расстояния между молекулами. Это объясняется увеличением межмолекулярного притяжения при росте энергии молекул. Изменение свойств жидкости связано с изменением коэффициента теплопроводности, вязкости и плотности.
Повышение температуры жидкости также может вызывать изменение ее фазового состояния. Некоторые жидкости при нагревании могут испаряться и превращаться в газ. Это происходит при достижении определенной температуры, которая называется температурой кипения. При нагревании жидкости ниже температуры кипения молекулы могут переходить в более энергичное состояние, но все еще оставаться в жидком состоянии.
Изменение свойств жидкости при нагревании играет важную роль в различных процессах, таких как кипячение, конденсация, дистилляция и т.д. Понимание этих процессов позволяет контролировать и использовать их в различных технологиях и промышленности.
Влияние температуры на реакции между молекулами
Когда жидкость нагревается, происходят различные химические и физические процессы, влияющие на взаимодействие молекул. Изменение температуры может значительно влиять на скорость и характер реакций между молекулами.
При повышении температуры, средняя кинетическая энергия молекул возрастает, что приводит к более интенсивным столкновениям и ускорению реакций. Это происходит из-за увеличения скорости движения молекул и повышения вероятности энергетических соударений.
Температура также может изменять энергетический барьер для реакции. Повышение температуры позволяет молекулам преодолеть этот барьер и увеличить вероятность успешного столкновения, что ведет к увеличению скорости реакции.
Однако при слишком высоких температурах также могут происходить и нежелательные реакции, включая распад или разрушение молекул, возникновение побочных продуктов и потерю структурных свойств жидкости. Поэтому важно подобрать оптимальную температуру для конкретной реакции.
Таблица ниже показывает общие изменения, которые происходят с молекулами при нагревании жидкости:
| Температура | Влияние на реакции между молекулами |
|---|---|
| Понижение | Замедление реакций. Меньшая вероятность столкновений между молекулами. |
| Умеренное повышение | Увеличение скорости реакций. Более интенсивные столкновения между молекулами. |
| Высокая | Быстрое увеличение скорости реакций. Увеличение вероятности успешного столкновения между молекулами. |
| Слишком высокая | Потеря структурных свойств. Распад или разрушение молекул. Побочные реакции. |
Понимание влияния температуры на реакции между молекулами позволяет улучшить процессы синтеза и превратить их в более эффективные и управляемые, что имеет большое значение для различных областей науки и технологии.



