Изомерия - это явление, при котором два или более органических соединений имеют одинаковую молекулярную формулу, но отличаются либо внутренней структурой, либо способом соединения атомов. Изомеры обладают различными свойствами и могут иметь различное действие на биологические системы.
Свойства изомеров зависят от расположения атомов и связей внутри молекулы. Часто различия между изомерами можно объяснить разной пространственной ориентацией атомов или групп атомов. Например, существуют изомеры, у которых атомы или группы атомов расположены по-разному вокруг двойных связей. Это может привести к различной реакционной активности и свойствам вещества.
Изомерия может проявляться и в рамках макромолекулярных структур. Например, у глюкозы существует несколько изомеров - альфа и бета-изомеры, которые отличаются растановкой группы гидроксилов в пространстве. Это приводит к различным свойствам этих изомеров и влияет на их роль в клеточном метаболизме.
Что такое изомерия

Изомерия представляет собой явление, при котором два или более химических соединения имеют одинаковую молекулярную формулу, но различаются в строении и свойствах. Такие соединения называются изомерами.
Изомерия является результатом различного пространственного расположения атомов в молекуле. Изомеры могут отличаться расположением атомов в пространстве, последовательностью связей между атомами или наличием функциональных групп.
Изомерия широко распространена в органической химии и играет важную роль в определении свойств и реакционной способности соединений. Изомеры могут различаться в физических свойствах, таких как температура плавления и кипения, растворимость и плотность, а также в химических свойствах, включая способность к реакциям и энергию активации.
Изомерия имеет применение в различных областях науки и промышленности, включая фармацевтику, пищевую промышленность, полимеры и материаловедение. Изучение изомерии позволяет углубленно понять законы и принципы химической связи и структуры вещества.
Определение и сущность изомерии

Суть изомерии заключается в том, что одна и та же молекула может быть организована по-разному. Это может быть связано с разной последовательностью атомов, их пространственным расположением или способом соединения. Различные типы изомерии включают структурную изомерию, геометрическую (конфигурационную) изомерию и оптическую изомерию.
Изомеры играют важную роль в органической химии и биохимии, поскольку они имеют разные свойства и могут вести себя по-разному в химических реакциях. Изучение изомерии позволяет лучше понять структуру и свойства органических соединений и применить это знание для синтеза новых веществ с определенными свойствами.
Важно отметить, что изомеры не всегда одинаково стабильны. Некоторые изомеры могут быть более стабильными и доминировать в конкретных условиях, в то время как другие могут быть менее стабильными и присутствовать в меньших количествах.
Типы изомерии
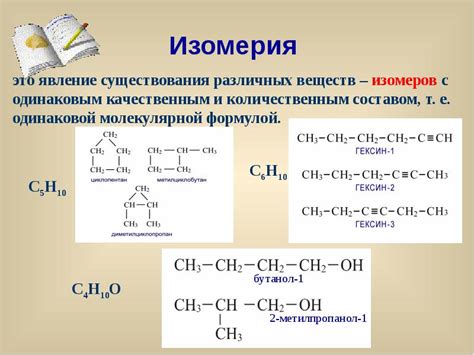
- Структурная изомерия:
- Цепная изомерия: Основана на различии в последовательности и связи атомов углерода в молекулах. Например, нормальный пропан и изобутан являются цепными изомерами.
- Позиционная изомерия: Отличается расположением или замещением функциональной группы в молекуле. Например, изомерия позиции двух и трех хлоробутана, где хлор присоединен к разным углеродным атомам в цепи.
- Функциональная изомерия: Связана с наличием разных функциональных групп в молекуле. Например, этиловый спирт и метиловый эфир являются функциональными изомерами.
- Конфигурационная изомерия: Обусловлена различием в расположении атомов в пространстве. Например, Z-изомер и E-изомер бутадиена - конфигурационные изомеры.
- Оптическая изомерия: Связана с способностью соединений вращать плоскость поляризованного света. Два оптически активных изомера, существующие в право- и левовращающих формах, называются энантиомерами.
Все эти типы изомерии подтверждают фундаментальные принципы химии - один и тот же набор атомов может образовывать различные соединения с разными свойствами и функциями в организмах и промышленности.
Примеры изомерии в органической химии
- Структурная изомерия: в этом виде изомерии атомы органического соединения располагаются по-разному, что приводит к различным химическим свойствам. Например, у бутилового спирта и изобутилового спирта одинаковая молекулярная формула C₄H₁₀О, но их строение отличается.
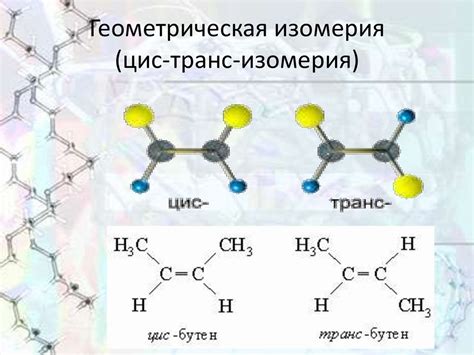
- Геометрическая изомерия: этот вид изомерии возникает, когда в молекуле присутствуют две или более двойные связи и атомы или группы атомов расположены по-разному относительно плоскости молекулы. Например, цис- и транс-изомеры будут иметь различные свойства и могут образовываться при геометрической изомерии алкенов.
- Оптическая изомерия: это изомерия, связанная с наличием хиральных центров в молекуле. Оптические изомеры не могут быть суперпонижены друг на друга и могут образовываться, например, в аминокислотах.
- Татиоизомерия: это изомерия, которая характерна для соединений, содержащих атомы серы. Татиоизомерия может проявиться в различном расположении атомов серы в молекуле и может встречаться, например, в соединениях тиолов и сульфидов.
Это лишь некоторые примеры изомерии, и в органической химии существует множество других видов изомерии, которые способствуют богатству и разнообразию органических соединений.



