Константа скорости химической реакции является важным понятием, которое позволяет определить, насколько быстро или медленно происходит определенный химический процесс. Измерение этой константы помогает более полно понять и описать химическую реакцию. Она может быть выражена в различных единицах измерения, которые играют важную роль в химической науке.
Константа скорости химической реакции обычно обозначается как "k" и определяется как скорость реакции, деленная на концентрацию реагентов. Измерение константы скорости происходит во время эксперимента по химической реакции. Это позволяет исследователям получить информацию о скорости реакции в различных условиях и о влиянии различных факторов на скорость химической реакции.
Различные единицы измерения используются для выражения константы скорости химической реакции в зависимости от типа реакции и используемых реагентов. Например, для реакции первого порядка константа скорости имеет единицы времени в степени минус один (-1). Такие единицы как секунда в степени минус один на реакцию считается общепринятыми. Для более сложных реакций, константы скорости измеряются в более специфических единицах, которые отражают особенности данного типа реакции.
Понятие и значение константы скорости
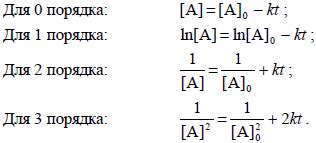
Константа скорости обычно обозначается символом k и имеет определенные единицы измерения. Размерность константы скорости зависит от общей степени реакции и порядка реакции, которые определены экспериментально.
Значение константы скорости важно для понимания и изучения химических реакций. Она позволяет нам определить, какие факторы влияют на скорость реакции и как изменение условий может повлиять на протекание процесса. Кроме того, константа скорости позволяет предсказывать скорость реакции в различных условиях и проводить расчеты.
Знание константы скорости также позволяет изучать механизмы реакций, обнаруживать промежуточные стадии и взаимодействия между реагентами. Оно помогает улучшить производительность химических процессов и разработать эффективные методы синтеза в различных отраслях промышленности и науки.
Определение и принцип измерения
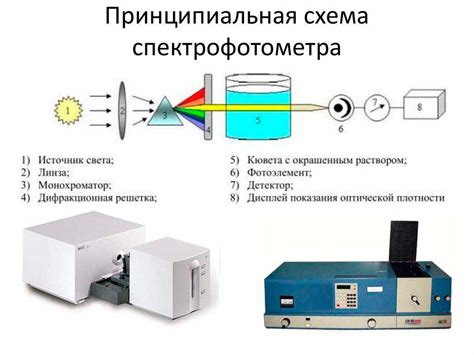
Для определения константы скорости химической реакции проводятся специальные эксперименты, в которых изменяются начальные условия реакции и измеряется изменение концентрации реагентов или продуктов в зависимости от времени. Принцип измерения константы скорости заключается в том, что скорость реакции можно определить, измерив, как быстро меняется концентрация реагентов или продуктов реакции в единицу времени. Математически это выражается уравнением, известным как уравнение скорости реакции.
Для измерения константы скорости химической реакции используются различные методы, в зависимости от характеристик реакции и доступных инструментов. Одним из основных методов является спектрофотометрия, при которой измеряется поглощение света реакционной смесью в зависимости от времени. Этот метод особенно эффективен при реакциях, в которых реагенты или продукты реакции имеют цвет.
Другим распространенным методом измерения константы скорости является газовая хроматография. При этом методе анализируется состав газовой фазы реакционной смеси с помощью специального прибора. Газовая хроматография позволяет определить концентрации реагентов и продуктов реакции в зависимости от времени.
- Спектрофотометрия
- Газовая хроматография
Определение константы скорости позволяет установить зависимость скорости химической реакции от начальных условий и концентраций реагентов. Эти данные могут быть использованы для оптимизации условий проведения химических процессов, контроля качества продукции и разработки новых реакционных механизмов.
Единицы измерения и их связь с константой скорости
Единицы измерения константы скорости зависят от порядка реакции. В общем виде, единицы измерения для различных порядков реакции (n) представлены в таблице:
| Порядок реакции | Единицы измерения константы скорости (k) |
|---|---|
| n=0 | с-1 |
| n=1 | с-1 |
| n=2 | М-1·с-1 |
| n=3 | М-2·с-1 |
Видно, что для реакций нулевого и первого порядка единицы измерения константы скорости являются обратными секундам (с-1). Для реакций второго порядка единицы измерения константы скорости включают единицы концентрации (моль на литр), так как порядок реакции включает концентрации реагентов. Для реакций третьего порядка добавляется еще одна единица концентрации.
Знание единиц измерения константы скорости помогает сравнивать скорости разных реакций и оценивать их быстроту. Также, зная константу скорости, можно предсказать, как изменится скорость реакции при изменении концентрации реагентов или температуры.



