Кинетическая энергия молекул - это энергия, связанная с их движением. Она определяет температуру и состояние вещества. Но что конкретно влияет на среднюю кинетическую энергию молекул?
Во-первых, масса молекул играет важную роль. Чем больше масса молекулы, тем меньше скорость ее движения и, соответственно, меньше ее кинетическая энергия. Например, вода имеет меньшую среднюю кинетическую энергию, чем аммиак, потому что масса молекулы воды больше.
Во-вторых, температура также оказывает влияние на среднюю кинетическую энергию молекул. Чем выше температура, тем больше скорость движения молекул, и, следовательно, выше их кинетическая энергия. Таким образом, при нагревании вещества, его кинетическая энергия повышается.
Наконец, агрегатное состояние вещества также определяет среднюю кинетическую энергию его молекул. В газообразном состоянии молекулы находятся в постоянном движении с высокой скоростью, поэтому их кинетическая энергия выше, чем у молекул в жидком или твердом состоянии. В жидкости молекулы движутся медленнее, а в твердом состоянии они практически неподвижны, поэтому средняя кинетическая энергия этих веществ ниже.
Масса молекул и их скорость

Средняя кинетическая энергия молекул вещества напрямую зависит от их массы и скорости. Молекулы с меньшей массой имеют более высокую среднюю кинетическую энергию, чем молекулы с большей массой при одинаковых скоростях.
Масса молекул является важным фактором определения средней кинетической энергии. Чем меньше масса молекулы, тем больше движение у неё. Например, молекулы водорода имеют малую массу и поэтому могут двигаться с большей скоростью по сравнению с молекулами более тяжёлого вещества, например, кислорода.
Скорость молекул также оказывает влияние на их среднюю кинетическую энергию. Молекулы с более высокой скоростью имеют большую кинетическую энергию. Влияние скорости на среднюю кинетическую энергию иллюстрируется термодинамическими законами, такими как закон Грэма. Закон Грэма устанавливает, что скорость молекулу газа пропорциональна обратному квадратному корню из её молекулярной массы.
Итак, масса молекул и их скорость взаимосвязаны и определяют среднюю кинетическую энергию молекул. Понимание этой связи позволяет более глубоко изучать физические свойства вещества и применять их в различных научно-технических отраслях.
Температура и термодинамические состояния

Чем выше температура, тем больше средняя кинетическая энергия молекул. Это означает, что молекулы движутся быстрее и имеют большую энергию, что приводит к более активному взаимодействию молекул.
Температура также влияет на фазовое состояние вещества. При достаточно низкой температуре вещество может находиться в твердом состоянии, где молекулы сильно связаны и практически не двигаются. При увеличении температуры вещество переходит в жидкое состояние, где молекулы двигаются более свободно. При еще большей температуре вещество может перейти в газообразное состояние, где молекулы движутся весьма свободно.
Температура измеряется в градусах и может быть измерена с помощью различных термометров. Одним из наиболее распространенных способов измерения температуры является использование шкалы Цельсия или Кельвина.
Таким образом, температура является фундаментальной величиной, определяющей физические свойства вещества и термодинамические состояния системы. Она влияет на среднюю кинетическую энергию молекул и фазовое состояние вещества, при этом измеряется в градусах и может быть измерена с помощью различных термометров.
Движение в трехмерном пространстве
В трехмерном пространстве молекулы движутся со скоростью по трем осям координат - x, y и z. Это означает, что каждая молекула имеет три составляющих скорости - vx, vy и vz. Сумма этих составляющих скоростей определяет абсолютную скорость молекулы.
Для анализа движения молекул в трехмерном пространстве удобно использовать таблицу, в которой отображаются значения составляющих скоростей. Такая таблица позволяет наглядно представить величину и направление скорости каждой молекулы.
| Молекула | vx (м/c) | vy (м/c) | vz (м/c) |
|---|---|---|---|
| Молекула 1 | 5 | 2 | 3 |
| Молекула 2 | -3 | 0 | 1 |
| Молекула 3 | 1 | 4 | -2 |
Зная значения составляющих скоростей для каждой молекулы, можно рассчитать их абсолютные скорости и среднюю кинетическую энергию. Средняя кинетическая энергия может быть вычислена как среднее значение кинетических энергий всех молекул в системе.
Таким образом, движение молекул в трехмерном пространстве играет важную роль в определении их средней кинетической энергии. Комбинированные значения скоростей молекул по осям координат представляют собой векторную величину, которая является основой для расчета средней кинетической энергии системы молекул.
Законы сохранения энергии
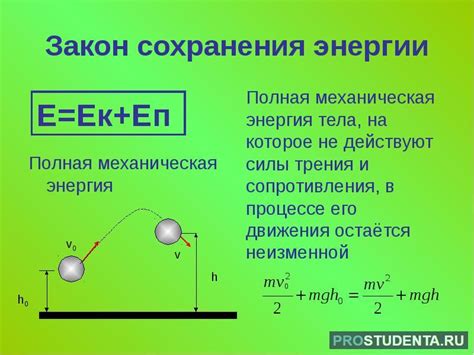
Средняя кинетическая энергия молекул вещества также подчиняется законам сохранения энергии. Процесс преобразования энергии между частицами вещества происходит в результате их взаимодействия друг с другом.
Закон сохранения энергии молекулярного движения утверждает, что сумма кинетических энергий молекул вещества остается неизменной при условии отсутствия внешних воздействий. Это означает, что если одна молекула приобретает дополнительную кинетическую энергию, то другая молекула должна потерять такую же энергию, чтобы общая сумма осталась постоянной.
Закон сохранения энергии теплового движения утверждает, что средняя кинетическая энергия молекул вещества пропорциональна их абсолютной температуре. Это означает, что при повышении температуры средняя кинетическая энергия молекул увеличивается, а при понижении - уменьшается.
Тип вещества и его физические свойства

Тип вещества и его физические свойства существенно влияют на среднюю кинетическую энергию молекул. Определение этой энергии связано с температурой вещества и его массой. Кинетическая энергия молекул определяется их скоростью и массой.
Температура - это мера средней кинетической энергии молекул вещества. Чем выше температура, тем выше средняя кинетическая энергия молекул и их скорость. Молекулы вещества при повышении температуры начинают двигаться более быстро, что приводит к увеличению их средней кинетической энергии.
Масса молекулы также важна для определения средней кинетической энергии. Чем меньше масса молекул, тем выше их скорость и, соответственно, средняя кинетическая энергия. Это связано с прямой зависимостью между скоростью молекулы и ее кинетической энергией: чем выше скорость, тем больше кинетическая энергия молекулы.
Тип вещества также влияет на среднюю кинетическую энергию молекул. Различные вещества имеют разные физические свойства, такие как межмолекулярные силы, внутренняя структура и точка кипения. Вещества с сильными межмолекулярными силами будут иметь молекулы, движущиеся с меньшей скоростью и, соответственно, ниже среднюю кинетическую энергию.
Кроме того, молекулы веществ с более сложной внутренней структурой, таких как полимеры, будут обладать большей массой и более медленными скоростями, что приводит к снижению средней кинетической энергии. Точка кипения также влияет на среднюю кинетическую энергию молекул. Вещества с более высокой точкой кипения будут иметь молекулы с более низкими скоростями и меньшей средней кинетической энергией.
Таким образом, тип вещества и его физические свойства играют важную роль в определении средней кинетической энергии молекул.
Средняя свободная длина пробега молекул

Свободная длина пробега молекул зависит от таких параметров, как плотность газа, давление, температура и степень сжатия газа. Чем выше плотность газа или давление, тем меньше будет свободная длина пробега молекул. В то же время, при повышении температуры или уменьшении степени сжатия газа, свободная длина пробега молекул увеличивается.
Средняя свободная длина пробега молекул может быть вычислена с помощью следующей формулы:
- Вычислите средний объем, занимаемый одной молекулой газа в состоянии равновесия.
- Вычислите среднюю длину свободного пробега молекулы, используя объем и плотность газа.
- Учитывая степень сжатия газа, приведите полученную длину к исходному объему газа.
Средняя свободная длина пробега молекул является важной характеристикой газа и позволяет осуществлять оценку его транспортных свойств. Знание этого параметра позволяет улучшить проектирование и эффективность различных систем и устройств, работающих на основе газа.
Межмолекулярные взаимодействия
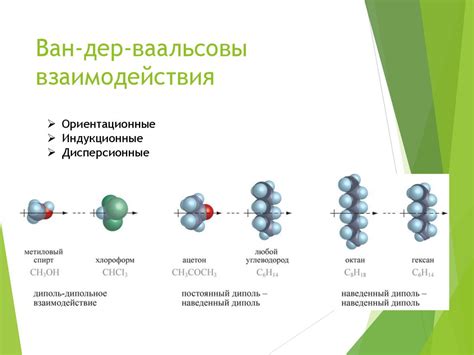
Средняя кинетическая энергия молекул вещества определяется не только их скоростью, но и межмолекулярными взаимодействиями. В зависимости от типа вещества, эти взаимодействия могут быть различной природы.
Одним из самых распространенных типов межмолекулярных взаимодействий является взаимодействие Ван-дер-Ваальса. Оно происходит между неполярными молекулами и основано на появлении временных диполей в молекулах под воздействием соседних частиц. Эти временные диполи вызывают притяжение между молекулами и способствуют образованию жидкостей и твердых тел.
Для полярных молекул характерны силы Кулона - притяжение или отталкивание между заряженными частичками. Эти взаимодействия играют важную роль в растворах и приводят к образованию водородных связей, которые существенно влияют на свойства многих веществ, таких как вода.
Кроме того, кинетическую энергию молекул могут определять и другие межмолекулярные взаимодействия, такие как ионно-дипольные и дипольные взаимодействия. Они возникают, когда происходит взаимодействие между заряженными частицами и полярными молекулами соответственно.
Таким образом, межмолекулярные взаимодействия играют ключевую роль в определении средней кинетической энергии молекул вещества. Понимание этих взаимодействий позволяет объяснить не только физические свойства вещества, но и его химическую реакционную способность.
Настройка чувствительных элементов измерительной аппаратуры
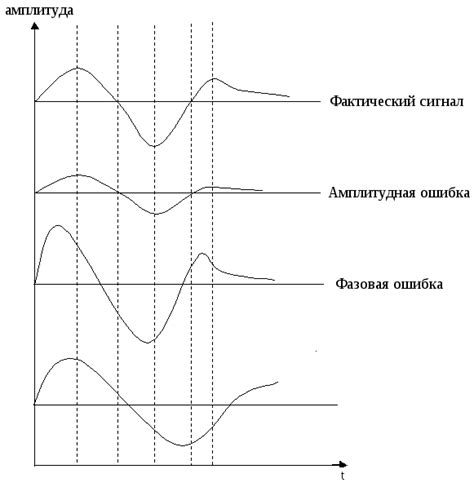
Чувствительные элементы в измерительной аппаратуре играют важную роль в определении средней кинетической энергии молекул. Точность измерений и надежность результатов зависят от правильной настройки этих элементов. Настройка чувствительных элементов требует тщательного подхода и использования специализированных методик.
Первый шаг при настройке чувствительных элементов - проверка их работоспособности и калибровка. Это позволяет установить их точность и соответствие требуемым стандартам. Для этого используются проверочные сигналы или эталоны, которые обеспечивают измерение с высокой точностью.
Второй шаг - определение оптимальных параметров работы чувствительных элементов. К ним относятся факторы, такие как частота измерений, диапазон измеряемых значений, уровень шума и погрешности измерения. Настройка с учетом этих параметров позволяет достичь максимальной чувствительности и стабильности работы аппаратуры.
Третий шаг - проведение калибровки и поверки настроенных чувствительных элементов. Это важный этап, который позволяет проверить точность измерений после настройки и убедиться в их соответствии установленным стандартам. Калибровка проводится с использованием эталонов, которые имеют известные значения и используются для сравнения.
Настройка чувствительных элементов измерительной аппаратуры - сложный процесс, требующий глубоких знаний и опыта. Правильная настройка позволяет получить точные и надежные результаты измерений, что особенно важно при определении средней кинетической энергии молекул.



