Газ – одна из основных составляющих вещества, обладающая определенным объемом и формой, но не имеющая постоянной формы и объема.
Газы встречаются в природе и являются неотъемлемой частью нашего окружающего мира. Они играют важную роль в химических реакциях и используются в различных промышленных процессах.
Главной особенностью газов является их высокая подвижность. Они распределяются равномерно в пространстве, заполняя имеющийся объем. Газы также обладают низкой плотностью, поэтому они могут существовать в виде облаков, паров или воздуха.
Основные свойства газов включают: объем, давление, температуру и количество вещества. Объем газа зависит от его температуры и давления. Чем выше температура или давление, тем больший объем газ занимает. В свою очередь, давление газа зависит от количества молекул, которые сталкиваются со стенками сосуда, в котором находится газ.
Газ в химии 8 класс: определение и свойства
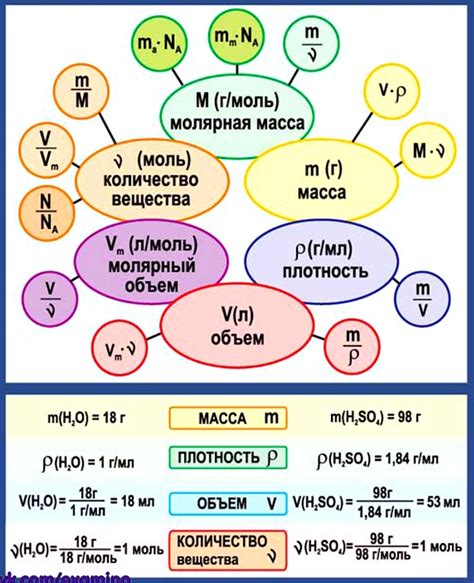
Газы имеют ряд характеристических свойств:
- Распределение по объему: газы не имеют определенной формы и заполняют все доступное пространство.
- Сжимаемость: газы могут сильно сжиматься под действием давления.
- Проницаемость: газы могут проникать сквозь маленькие отверстия и заполнять закрытые сосуды.
- Разреженность: газы имеют малую плотность и массу по сравнению с твердыми и жидкими веществами.
- Взаимодействие: газы легко смешиваются друг с другом и с другими веществами.
Газы в природе широко распространены, их можно встретить в атмосфере Земли, в составе жидкостей и твердых веществ. Многие химические реакции происходят именно с участием газообразных веществ.
Учебник по химии для 8 класса содержит основные сведения о газах, их свойствах и применении. Изучение газов важно для понимания принципов химических процессов и технологий.
Определение газа в химии
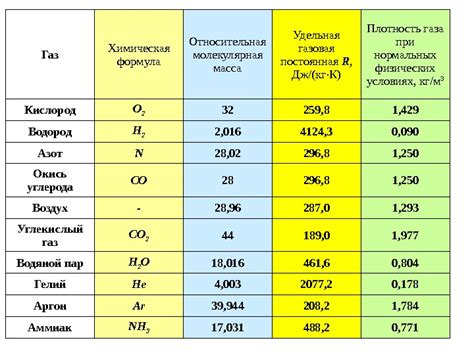
В химии газом называется одно из трех состояний вещества, помимо твердого и жидкого состояний. Газ обладает определенными свойствами, которые отличают его от других состояний вещества.
Газы обладают высокой подвижностью, так как их молекулы находятся в состоянии свободного движения и заполняют объем, в котором они находятся. Газы не имеют постоянной формы и объема, они могут легко изменять свою форму и объем под воздействием внешних условий, например, изменения температуры и давления.
Основные свойства газов включают:
- Компрессибельность: газы могут быть сжаты, уменьшая свои объемы под воздействием давления;
- Расширяемость: газы могут расширяться, увеличивая свои объемы, когда на них действует меньшее давление;
- Диффузия: газы способны перемешиваться между собой и с другими веществами в результате движения их молекул;
- Инертность: некоторые газы не проявляют химической активности и не вступают в реакции с другими веществами.
Газы играют важную роль в химических реакциях и применяются во множестве областей, включая промышленность, медицину, науку и технологии.
Физические свойства газов

Основные физические свойства газов:
| Свойство | Описание |
|---|---|
| Разрежимость | Газы характеризуются низкой плотностью и высокой подвижностью молекул, что позволяет им заполнять все доступное пространство. |
| Сжимаемость | Газы легко сжимаются под действием давления, при этом объем газа уменьшается, а плотность возрастает. |
| Расширяемость | При нагревании газов объем их увеличивается, что связано с возрастанием скорости движения молекул. |
| Диффузия | Газы способны распространяться по другим газам и растворяться в них благодаря случайным столкновениям молекул. |
| Давление | Газы оказывают давление на стенки сосудов, а его величина зависит от числа и энергии столкновений молекул. |
Эти свойства газов обусловливают их важные применения в различных отраслях науки и техники.
Термодинамические свойства газов
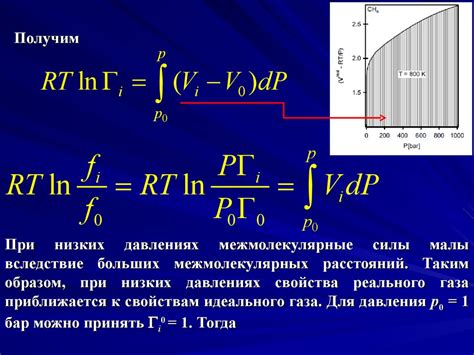
Газы обладают рядом уникальных термодинамических свойств, отличающих их от других агрегатных состояний вещества, таких как жидкость и твердое тело.
Одной из основных характеристик газов является сжимаемость. Газы могут быть сжаты в значительной степени при действии давления, что позволяет изменять их объем. При повышении давления объем газа уменьшается, а при понижении давления - увеличивается.
Другим важным свойством газов является их способность разбираться. Газы имеют низкую плотность по сравнению с жидкостями и твердыми телами, что позволяет им заполнять всю доступную им объем герметичного сосуда.
Еще одним значимым термодинамическим свойством газов является их способность к расширению и сжатию в зависимости от температуры. При нагревании, газы обычно расширяются, занимая больший объем, а при охлаждении сжимаются, занимая меньший объем.
Таким образом, термодинамические свойства газов, такие как сжимаемость, способность к разбиранию и зависимость от температуры, играют существенную роль в их поведении и важны при изучении химии газов.
Химические свойства газов
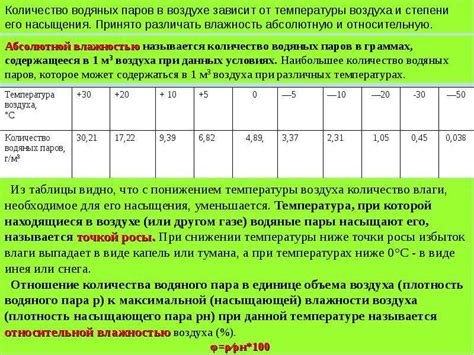
1. Газы обладают высокой диффузией. Это означает, что молекулы газа могут перемещаться с одного места на другое, заполняя имеющееся пространство. Благодаря этой свойству газы смешиваются быстро и равномерно.
2. Газы обладают высокой сжимаемостью. Это свойство позволяет изменять объем газа под воздействием давления. Газ можно сжать или расширить без изменения его химических свойств.
3. Газы обладают хорошей растворимостью в других газах и жидкостях. Газы могут растворяться в других газах или жидкостях, образуя гомогенные смеси. Растворимость газов зависит от давления и температуры.
4. Газы могут взаимодействовать химически с другими веществами. Например, газы могут гореть или проявлять реактивность с другими элементами. Под воздействием определенных условий, газы могут образовывать химические соединения или претерпевать разложение.
5. Большая часть газов обладает низкой плотностью и малым весом. Из-за своей низкой плотности газы воздушных смесей восходят наверх, в отличие от жидкостей и твердых веществ.
Описанные выше химические свойства газов имеют важное значение в различных процессах и явлениях, связанных с использованием газов в промышленности, научных исследованиях и повседневной жизни.
Применение газов в химии

В химии газы применяются в различных областях и процессах, например:
1. Реакции газов
Газы используются в химических реакциях в качестве реагентов или продуктов. Некоторые газы вступают в реакцию с другими веществами и образуют новые соединения. Например, при сжигании углеводородов воздухом выделяется углекислый газ (СО2).
2. Анализ газов
Газы могут быть использованы для анализа различных веществ. Например, в газоанализе измеряются концентрации газов в смеси, что помогает определить характеристики вещества. Газоанализ широко применяется в медицине, экологии и промышленности.
3. Транспортировка газов
Газы могут быть транспортированы по трубопроводам или в специальных емкостях. Это позволяет использовать газы в различных промышленных процессах, таких как производство электроэнергии, металлургия и химическая промышленность.
4. Создание условий для проведения реакций
Газы могут быть использованы для создания определенных условий в химических реакциях. Например, газы могут быть использованы для создания атмосферы определенного давления и состава, что может изменить скорость и направление реакции.
Таким образом, газы играют важную роль в химии и применяются в различных областях. Изучение свойств газов и их реакций помогает понять многочисленные явления и процессы, происходящие в химических системах.



