Фосфаты – это класс химических соединений, которые играют важную роль в жизни всех организмов. Они являются основными компонентами ДНК, РНК и АТФ, а также входят в состав костей и зубов. В химии 8 класса учащиеся знакомятся с основными свойствами и некоторыми представителями этого класса соединений.
Фосфаты образуются при соединении атомов фосфора с кислородом. Одним из наиболее распространенных фосфатов является фосфатная кислота (H3PO4), которая имеет несколько степеней окисления фосфора. Фосфатные ионы, такие как H2PO4- и HPO4^2-, являются основными составляющими фосфатной кислоты.
Фосфаты обладают рядом уникальных свойств. Они обладают высокой степенью растворимости в воде, что делает их доступными для усвоения организмом. Кроме того, фосфаты являются хорошими донорами энергии в химических реакциях и участвуют в обмене веществ в клетках.
Изучение фосфатов в химии 8 класса позволяет ученикам более глубоко понять роль этих соединений в живых организмах, а также ознакомиться с методами получения и применения фосфатов в различных отраслях промышленности и науки.
Определение фосфатов в химии 8 класс
В химии 8 класса фосфаты изучаются в рамках темы "Химические свойства солей". Они представляют собой одну из групп солей, которые образуются при реакции кислоты с щелочью. При этом вместо катиона в соли возникает замещение на ион фосфата (PO43-).
Фосфаты обладают следующими свойствами:
- Водахарактер солей
- Белые кристаллические вещества
- Растворимы в воде
- Образуют осадки солями кальция и свинца
- Имеют высокую химическую активность
Фосфаты имеют широкое применение в различных областях. Например, фосфаты кальция входят в состав костей и зубов и необходимы для их формирования и укрепления. Также фосфаты используются в производстве удобрений, стекла и моющих средств.
Свойства и применение фосфатов в химии 8 класс
Одно из главных свойств фосфатов - их растворимость в воде. Большинство фосфатов хорошо растворяются в воде, что делает их доступными для использования в различных химических реакциях и процессах. Они также обладают высокими тепловыми и химическими стабильностью, что делает их надежными и устойчивыми соединениями.
Фосфаты играют важную роль в биологических системах. Например, они являются важной частью ДНК и РНК - нуклеиновых кислот, отвечающих за передачу и хранение генетической информации. Они также являются ключевыми компонентами митохондрий - органелл, отвечающих за производство энергии в клетке.
В сельском хозяйстве фосфаты используются в качестве удобрений для повышения урожайности почвы. Они обеспечивают растения необходимыми питательными веществами, такими как фосфор, который является необходимым для роста и развития растений.
В промышленности фосфаты используются для производства моющих средств, дезинфицирующих средств, лакокрасочных материалов и прочих химических продуктов. Они также могут использоваться в качестве стабилизаторов, регуляторов pH и антиоксидантов.
| Применение | Примеры фосфатов |
|---|---|
| Удобрения | Суперфосфат, аммонийный фосфат |
| Производство моющих средств | Триполифосфат натрия |
| Производство лакокрасочных материалов | Фосфаты кальция, цинка и др. |
Таким образом, фосфаты имеют множество свойств и применений в различных областях химии, биологии, сельском хозяйстве и промышленности. Изучение и понимание этих соединений поможет учащимся 8 класса лучше понять мир химии и его роль в нашей жизни.
Реакции фосфатов в химии 8 класс
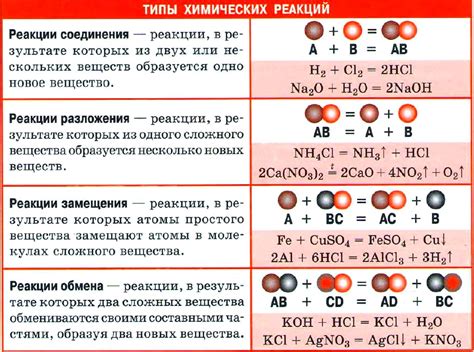
- Гидролиз фосфатов. Фосфаты могут подвергаться гидролизу при взаимодействии с водой. В результате этой реакции образуются ионы фосфата и ионы водорода. Примером такой реакции является гидролиз фосфата натрия:
- Образование кислот. Фосфаты способны образовывать кислоты при взаимодействии с кислотными оксидами. Например, фосфат кальция и серная кислота могут реагировать следующим образом:
- Образование соединений. Фосфаты могут реагировать с различными элементами и соединениями для образования новых соединений. Например, реакция фосфата натрия с кальцием приводит к образованию фосфата кальция:
Na3PO4 + H2O → NaOH + H3PO4
Ca3(PO4)2 + 3H2SO4 → 3 CaSO4 + 2H3PO4
Na3PO4 + CaCl2 → Ca3(PO4)2 + 6NaCl
Это лишь некоторые примеры реакций, в которых участвуют фосфаты. Они играют важную роль в химических процессах и имеют широкое применение в различных областях, включая пищевую промышленность, сельское хозяйство и медицину.



