Агрегатное состояние вещества - это одно из основных свойств материи, которое определяется макроскопическими характеристиками: формой, объемом и плотностью. Всего существует три основных агрегатных состояния: твердое, жидкое и газообразное. Каждое состояние обладает своими уникальными свойствами и характеризуется определенным уровнем упорядоченности молекул вещества.
Твердое состояние характеризуется тем, что молекулы вещества находятся в плотной упорядоченной структуре. Они колеблются вокруг своих положений равновесия, но не меняют свое расположение. Одним из главных свойств твердого состояния является его форма, которая остается неизменной при изменении условий окружающей среды.
Жидкое состояние вещества отличается от твердого тем, что молекулы находятся в более свободном состоянии. Они могут перемещаться друг относительно друга и не имеют фиксированных положений. В жидком состоянии вещество принимает форму сосуда, в котором оно находится, а также может изменять свой объем. Жидкости обладают свойством поверхностного натяжения и способностью капиллярного восхождения.
Наконец, газообразное состояние характеризуется высокой степенью хаотичности движения молекул. Они свободно перемещаются во всех направлениях и не имеют фиксированного положения. Газы не имеют определенной формы и объема, они полностью заполняют доступное пространство. Газообразное состояние вещества также характеризуется низкой плотностью и высокой подвижностью частиц.
Чем отличается твердое, жидкое и газообразное состояние?
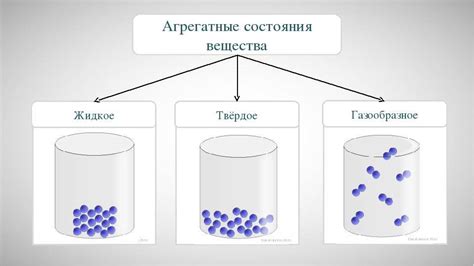
- Твердое состояние: В твердом состоянии молекулы вещества сцеплены между собой и имеют низкую энергию движения. Они имеют определенную форму и объем, не изменяющуюся при изменении условий окружающей среды. В твердом состоянии молекулы обычно расположены в регулярном упорядоченном макроскопическом пространственном расположении.
- Жидкое состояние: В жидком состоянии молекулы вещества относительно свободно движутся, но все же имеют некоторую сцепленность. Вода – типичный пример жидкого состояния, где молекулы не имеют фиксированного расположения, но все же они ближе друг к другу, чем в газообразном состоянии. Жидкое состояние не имеет определенной формы, но имеет определенный объем.
- Газообразное состояние: В газообразном состоянии молекулы вещества движутся свободно и не имеют сцепленности друг с другом. Газы заполняют все доступное им пространство и не имеют ни определенной формы, ни определенного объема. Газообразное состояние веществ может быть легко изменено изменением температуры или давления.
Таким образом, различия между твердым, жидким и газообразным состояниями заключаются в плотности и движении молекул, а также в их степени взаимодействия и упорядоченности.
Кристаллическая структура
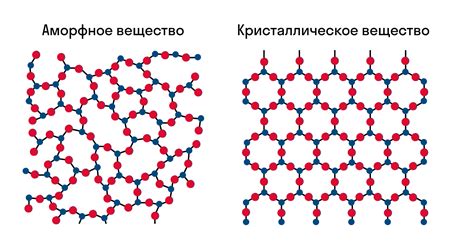
Кристаллическая структура имеет своеобразные свойства, такие как симметрия и определенное пространственное расположение атомов или молекул. Вещества с кристаллической структурой обычно обладают регулярной формой и складываются из множества одинаковых элементов, называемых элементарными ячейками.
Кристаллическое состояние является наиболее упорядоченным агрегатным состоянием вещества. Все кристаллы имеют свою характерную форму и ростут в определенном направлении. Например, соль в кристаллической форме образует прозрачные кубические кристаллы, алмаз имеет гранаты, а снег образует хаотические кристаллы с шестиугольными фигурами.
Кристаллическая структура определяет многие свойства вещества, такие как его твердость, показатели преломления света и теплоемкость. Кристаллы также могут оказывать влияние на химическую активность вещества и его способность образовывать соединения с другими веществами.
Кристаллическая структура играет важную роль в различных отраслях науки и техники. Она используется в материаловедении для разработки новых материалов с определенными свойствами, в кристаллохимии для исследования структуры и свойств химических соединений, а также в кристаллографии для определения структуры кристаллов с помощью рентгеновской дифракции.
Силы притяжения
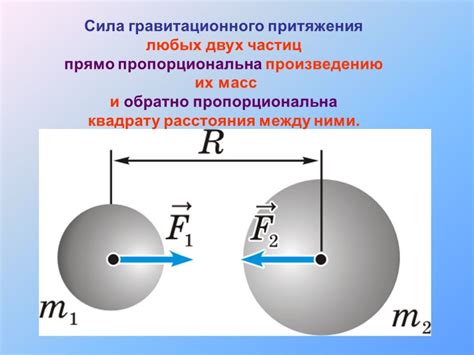
В твердом состоянии силы притяжения между частицами вещества настолько сильны, что они остаются на своих местах и не могут перемещаться. В жидком состоянии силы притяжения между частицами слабее, что позволяет им свободно перемещаться друг относительно друга. В газообразном состоянии силы притяжения между частицами минимальны, что позволяет им свободно перемещаться во всех направлениях.
Силы притяжения определяют также плотность вещества. В твердом состоянии плотность вещества обычно самая высокая, так как частицы в этом состоянии находятся на своих местах и тесно упакованы друг относительно друга. В жидком состоянии плотность вещества ниже, так как частицы могут свободно перемещаться и устраиваться в слоях. В газообразном состоянии плотность вещества наименьшая, так как частицы находятся на большом расстоянии друг от друга и перемещаются в пространстве.
Силы притяжения также определяют физические свойства вещества в различных состояниях. Например, в твердом состоянии вещество обладает определенной формой и объемом, в жидком состоянии – не имеет определенной формы, но обладает определенным объемом, а в газообразном состоянии – не имеет определенной формы и объема, заполняет все доступное пространство.
Форма и объем

Твердые тела обладают определенной формой и объемом. Они сохраняют свою форму, не зависимо от того, в какое место или сосуд они помещены. Твердые тела характеризуются определенной структурой внутреннего строения, в котором молекулы или атомы расположены плотно и организованно. Примерами твердых тел являются лед, металлы, камни и многие другие материалы.
Жидкости, в отличие от твердых тел, не имеют определенной формы, но они имеют определенный объем. Жидкости имеют способность принимать форму сосуда, в котором они находятся, и сохранять свой объем. Молекулы или атомы жидкости расположены достаточно близко друг к другу, но не настолько плотно, как в твердых телах. Например, вода, спирт, масло - все это жидкости.
Газы, в отличие от твердых тел и жидкостей, не имеют определенной формы и объема. Они способны заполнять всю доступную им область. Молекулы или атомы газов находятся на больших расстояниях друг от друга и могут свободно перемещаться. Воздух, кислород, углекислый газ - примеры газовых состояний.
Тепловое движение

Тепловое движение приводит к тому, что частицы вещества располагаются в определенных агрегатных состояниях: твердом, жидком и газообразном. Так, в твердом состоянии частицы находятся практически на месте, но продолжают совершать колебательные движения вокруг своих положений равновесия.
В жидком состоянии силы притяжения между частицами уже недостаточны для зафиксированного положения, поэтому они могут перемещаться, подражая друг другу. Однако, жидкость сохраняет объем, но приобретает форму сосуда, в котором она находится.
В газообразном состоянии, частицы совершают более энергичные движения, сталкиваются и отскакивают друг от друга. Газы не имеют фиксированной формы и объема, а заполняют все доступное пространство.
Таким образом, агрегатное состояние вещества определяется интенсивностью теплового движения частиц – чем выше температура, тем энергичнее движение частиц и менее устойчивая форма и объем вещества.
Плотность

Плотность может значительно отличаться в разных состояниях вещества. Например, у твердых веществ плотность обычно выше, чем у жидкостей и газов. Это связано с более плотной упаковкой атомов или молекул в твердом состоянии.
В жидком состоянии плотность вещества обычно ниже, так как атомы или молекулы могут свободно двигаться и смещаться внутри жидкости. Это позволяет жидкостям принимать форму сосуда, в котором они находятся.
Плотность газов является наименьшей из всех трех состояний вещества, так как атомы или молекулы газов очень далеко друг от друга и могут свободно двигаться в пространстве.
Плотность является важной характеристикой вещества, так как она может влиять на его свойства и поведение. Например, плотность может влиять на плавучесть твердых тел в жидкостях, на плотность воздуха и его способность задерживать тепло.
Изменение состояния
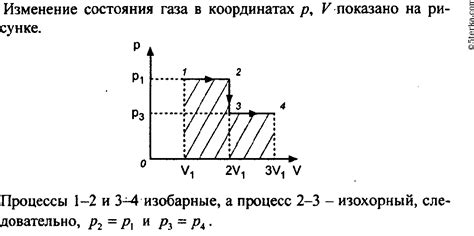
Агрегатное состояние вещества может изменяться под воздействием различных факторов, таких как температура и давление.
Изменение температуры оказывает наибольшее влияние на агрегатное состояние. При повышении температуры, вещество может переходить из одного состояния в другое. Например, при нагревании твердого вещества, оно может стать жидким, а затем газообразным. Наоборот, при охлаждении газообразного вещества оно может конденсироваться и стать жидким, а затем твердым.
Также, изменение давления может влиять на агрегатное состояние вещества. При повышении давления, некоторые газообразные вещества могут конденсироваться и стать жидкими или твердыми. Наоборот, при снижении давления, жидкости могут испаряться и стать газообразными.
Изменение состояния вещества можно наблюдать в повседневной жизни. Например, при варке воды, она начинает кипеть и превращается в пар. При охлаждении пара, он конденсируется и превращается в капли воды.
Ознакомившись с факторами, влияющими на агрегатное состояние вещества, можно лучше понять многообразие явлений, которые наблюдаются в природе и в ежедневной жизни.



