Крекинг – один из важных процессов в химии, который позволяет получить более ценные продукты из более простых и дешевых исходных материалов. Крекинг используется в нефтеперерабатывающей и химической промышленности для переработки нефти и углеводородных веществ.
Процесс крекинга основан на разрыве крупных молекул углеводородов на более маленькие и более активные. Это позволяет получить большее количество продуктов с более низкими молекулярными массами, которые могут быть использованы для производства пластмасс, бензина, дизельного топлива и других химических веществ.
В химии существует несколько видов крекинга, включая термический, катализаторный и гидрокрекинг. Термический крекинг осуществляется путем нагревания углеводородов до высокой температуры без использования катализаторов. Этот процесс часто проводится при давлении, чтобы увеличить выход более ценных продуктов.
Катализаторный крекинг – это процесс, при котором углеводороды нагреваются в присутствии катализаторов, которые ускоряют разрыв молекулярных связей. Это позволяет преобразовать более длинные углеводородные цепи в более короткие, что увеличивает выход более ценных продуктов.
Гидрокрекинг – это процесс крекинга, который осуществляется в присутствии водорода и катализаторов. В этом процессе углеводороды растворяются в водороде и затем разрываются при повышенной температуре и давлении. Гидрокрекинг часто используется для очистки тяжелых нефтей и получения более чистых и ценных продуктов.
Чем же является крекинг в химии?

Крекинг может происходить по различным механизмам. Одним из основных видов крекинга является термический крекинг, который осуществляется при высокой температуре и давлении. В результате этого процесса молекулы углеводородов разрываются на короткие фрагменты, которые затем могут быть использованы для получения более ценных продуктов.
Ещё одним видом крекинга является каталитический крекинг, который происходит при наличии катализатора. Катализатор помогает ускорить химическую реакцию и снизить её энергетическую стоимость. Каталитический крекинг широко применяется в нефтеперерабатывающей промышленности для получения бензина и других ценных продуктов из более тяжёлых нефтепродуктов.
Крекинг в химии является важным процессом, позволяющим получить более ценные и требуемые продукты из сырой нефти. Этот процесс постоянно совершенствуется и развивается, что позволяет улучшить качество и эффективность производства нефтепродуктов.
| Вид крекинга | Описание |
|---|---|
| Термический крекинг | Разрыв молекул углеводородов при высокой температуре и давлении. |
| Каталитический крекинг | Разрыв молекул углеводородов при наличии катализатора. |
Пиролиз и его роль в процессе крекинга
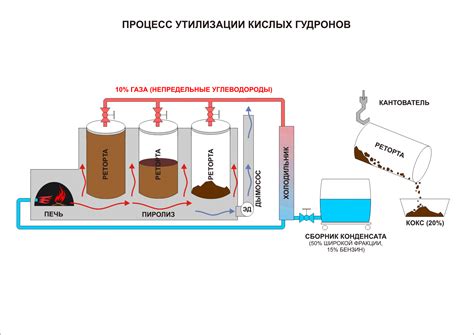
В процессе крекинга, сырье подвергается пиролизу, что позволяет разрушить длинные молекулы и создать кратковременные связи между атомами углерода. Такой разрыв молекул позволяет получить более легкие углеводороды, которые затем могут быть использованы в различных отраслях промышленности.
В зависимости от условий проведения крекинга, пиролиз может быть различным. Однако, его основной принцип – разложение длинных углеводородных цепей на более короткие, что позволяет получить ценные фракции продуктов.
Пиролиз обычно осуществляется при температурах от 400 до 800 градусов Цельсия и давлении от 1 до 10 атмосфер. При таких условиях происходит эффективное разложение молекул, и реагенты имеют возможность преобразоваться в более легкие компоненты.
Термокаталитический крекинг: некоторые особенности
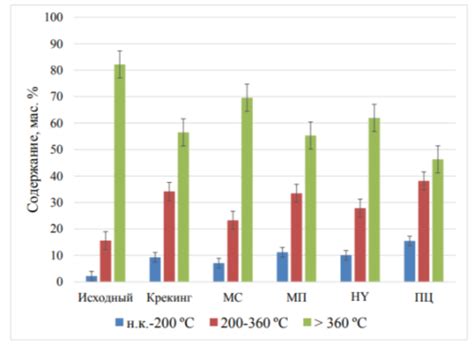
Особенностью термокаталитического крекинга является возможность контролируемого разрушения молекул углеводородов с целью получения необходимых фракций продуктов. Катализаторы, присутствующие в процессе, играют важную роль в оптимизации равновесия реакций и ускорении скорости разрушения молекул.
Данный метод крекинга применяется в производстве нефтепродуктов, таких как бензин, дизельное топливо и другие, а также в производстве различных органических соединений. Термокаталитический крекинг позволяет получить более ценные и востребованные фракции углеводородов из исходного сырья.
Активности катализаторов при парокрекинге
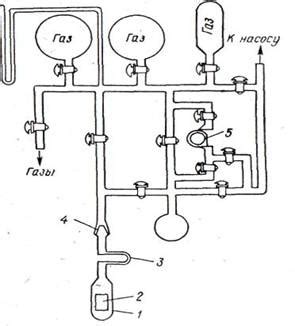
При парокрекинге применяются различные катализаторы, которые играют ключевую роль в процессе разрушения углеводородных молекул. Катализаторы помогают ускорить химические реакции, снижая активационную энергию и повышая эффективность процесса.
Одним из самых распространенных катализаторов при парокрекинге является катализатор ZSM-5, который представляет собой кристаллическую структуру с микропорами. Благодаря своей высокой поверхностной активности и размеру пор, этот катализатор позволяет проводить эффективное разрушение сложных углеводородных молекул.
Кроме катализатора ZSM-5, также используются другие катализаторы, такие как молибденит, крекинговые катализаторы на основе металлов (никель, платина, рений) и другие.
Активность катализаторов при парокрекинге зависит от их поверхностной активности, структуры, температуры и других факторов. Катализаторы должны быть эффективными в разрушении углеводородных молекул, что позволяет получать желаемые продукты в высоких количествах.
Катализаторы при парокрекинге могут быть как кислотными, так и основными. Кислотные катализаторы обладают способностью сцепляться с углеводородными молекулами и разрушать их на более маленькие фрагменты. Основные катализаторы, в свою очередь, способны образовывать межмолекулярные связи и проводить реакции конденсации.
В итоге, активность катализаторов при парокрекинге определяет эффективность процесса разрушения сложных углеводородных молекул и получения ценных продуктов, таких как бензин, дизельное топливо и другие углеводородные соединения.
Внимание крекинга: поверхностная и объемная кислотность

Кислотность крекинга может быть выражена двумя способами: поверхностной и объемной. Поверхностная кислотность определяет активность кислотных центров на поверхности катализатора, в то время как объемная кислотность характеризует общее количество кислотных центров внутри катализатора.
Поверхностная кислотность играет важную роль в реакциях крекинга, поскольку она определяет возможность молекул углеводородов реагировать с катализатором. Чем выше поверхностная кислотность, тем легче происходит реакция крекинга. Однако очень высокая поверхностная кислотность может привести к побочным реакциям, таким как дезактивация катализатора или образование кокса.
Объемная кислотность, с другой стороны, определяет общую активность катализатора и его способность разрушать молекулы углеводородов. Это связано с концентрацией кислотных центров внутри катализатора. Чем выше объемная кислотность, тем более эффективным будет процесс крекинга.
Поверхностная и объемная кислотность обычно взаимосвязаны: повышение поверхностной кислотности обычно приводит к увеличению объемной кислотности. Однако, для достижения оптимальных результатов крекинга необходимо балансировать оба этих параметра.



