ОГЭ по химии – это одно из самых важных испытаний для школьников, сдающих выпускные экзамены. Оно проверяет знания и навыки в области химии, которые являются основой для дальнейшего образования в этой науке. Чтобы успешно сдать ОГЭ по химии, нужно не только изучить необходимые темы, но и научиться правильно подготовиться к экзамену. В этой статье мы расскажем о секретах успешной сдачи ОГЭ по химии, подробно рассмотрим основные темы, а также дадим полезные советы для эффективной подготовки.
Перед тем как начать готовиться к ОГЭ по химии, стоит понять, что это экзамен, который требует серьезной подготовки. Ведь именно результаты ОГЭ могут повлиять на возможности поступления в желаемое учебное заведение. Первым шагом на пути к успешной сдаче ОГЭ по химии является осознание этой важности и принятие решения о серьезной подготовке.
Основные темы, которые необходимо изучить перед экзаменом, включают: атом и периодическая система химических элементов, химические свойства веществ, химические реакции, основные законы и принципы химии. Изучение этих тем позволит получить базовые знания, которые необходимы для успешной сдачи ОГЭ по химии. Кроме того, стоит уделить внимание решению задач, так как они являются неотъемлемой частью экзамена и требуют практических навыков учащегося.
Основные темы ОГЭ по химии

При подготовке к ОГЭ по химии необходимо уделить особое внимание изучению следующих тем:
1. Строение атома и периодическая система элементов
В этой теме необходимо изучить строение атома, атомный номер, массовый номер и электронную конфигурацию элемента. Также следует ознакомиться с периодической системой элементов и ее основными свойствами.
2. Химические связи и химические формулы
В этой теме рассматриваются различные типы химических связей (ионная, ковалентная, металлическая) и способы записи химических формул. Необходимо знать, как определить молекулярную и эмпирическую формулу вещества.
3. Растворы и их свойства
В этой теме изучаются свойства растворов, включая растворимость, концентрацию и нейтрализацию растворов кислот и щелочей. Также следует знать методы разделения смесей и способы получения растворов различной концентрации.
4. Кислоты, основания и соли
В этой теме изучаются свойства кислот, оснований и солей, а также их нейтрализационные реакции. Следует знать способы получения и источники кислот, оснований и солей, а также уметь определить их формулы и названия.
5. Окислительно-восстановительные реакции
В этой теме изучаются окислительно-восстановительные реакции и способы определения степени окисления элементов. Необходимо знать, как определить окислитель и восстановитель в реакции, а также уметь балансировать реакции с учетом изменения степени окисления.
Запомните, что успешная сдача ОГЭ по химии требует не только тщательной подготовки и освоения основных тем, но и умения решать задачи. Практикуйтесь в решении задач и тестовых заданий, чтобы уверенно справиться с экзаменом.
Атомы и молекулы

- Атом является основным строительным блоком вещества. Он состоит из ядра, которое содержит протоны и нейтроны, и электронной оболочки, на которой находятся электроны.
- Протоны имеют положительный заряд, а электроны – отрицательный. Нейтроны не имеют заряда.
- Атомы объединяются в молекулы. Молекула представляет собой устойчивую единицу вещества, состоящую из двух или более атомов, связанных химической связью.
- У разных элементов разное количество протонов, но они имеют одинаковое количество электронов, чтобы сделать заряд атома нейтральным.
- Атомы и молекулы могут образовывать различные химические соединения, которые имеют свои уникальные свойства и способности реагировать с другими веществами.
Химические реакции
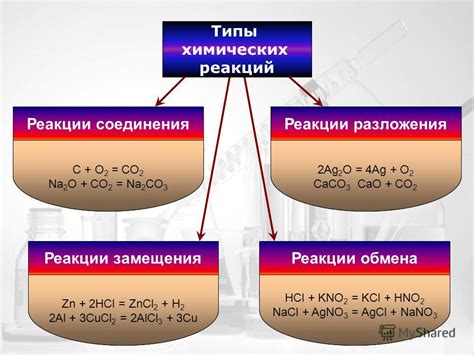
Химические реакции можно классифицировать по различным признакам. Одним из основных признаков являются исходные вещества и полученные продукты реакции. Реакции могут быть прямыми, обратимыми или обратимыми с обратной реакцией.
| Тип реакции | Пример |
|---|---|
| Синтез | 2Na + Cl2 = 2NaCl |
| Анализ | 2H2O = 2H2 + O2 |
| Диссоциация | HCl = H+ + Cl- |
| Нейтрализация | HCl + NaOH = NaCl + H2O |
| Окислительно-восстановительная | 2Na + Cl2 = 2NaCl |
| Комплексообразование | CuSO4 + 4NH3 = [Cu(NH3)4]SO4 |
При подготовке к экзамену по химии важно знать основные типы реакций и уметь их распознавать и сбалансировать. Для этого нужно практиковаться в решении задач и проведении лабораторных экспериментов.
Также стоит изучить основные понятия, связанные с реакциями, такие как стехиометрия, селективность, скорость реакции и энергия активации.
Правильная подготовка и усвоение материала по химическим реакциям поможет успешно сдать ОГЭ по химии и достичь хороших результатов.
Растворы и смеси

Один из ключевых моментов, который следует учесть при подготовке, - это знание процесса растворения вещества. Важно понимать, что растворение - это процесс взаимного проникновения молекул растворителя и растворяемого вещества. При этом растворимость вещества зависит от его химической природы и температуры.
Для определения концентрации раствора используют такие понятия, как массовая доля и объемная доля. Массовая доля растворителя - это отношение массы растворенного вещества к массе раствора. Объемная доля растворителя - это отношение объема растворителя к объему раствора.
Одной из ключевых тем является растворимость вещества. Растворимость - это способность вещества растворяться в определенном количестве растворителя при определенной температуре. Растворность вещества может зависеть от температуры и изменяться в зависимости от растворителя.
Важно также знать, как происходит растворение ионных и молекулярных веществ. Растворение ионных веществ сопровождается образованием ионов в растворе и их дальнейшим прохождением через вещества. Растворение молекулярных веществ происходит путем размножения молекул, которые взаимодействуют с молекулами растворителя.
Знание химических и физических свойств растворов также является важным аспектом подготовки к экзамену. Химические свойства растворов определяются способностью проходить химические реакции. Физические свойства растворов включают такие параметры, как температура кипения, плотность, вязкость и т.д.
Все эти темы следует изучить и усвоить перед экзаменом по химии ОГЭ. Регулярное повторение материала, решение задач и проведение экспериментов помогут хорошо подготовиться и успешно сдать экзамен.
Кислоты и основания
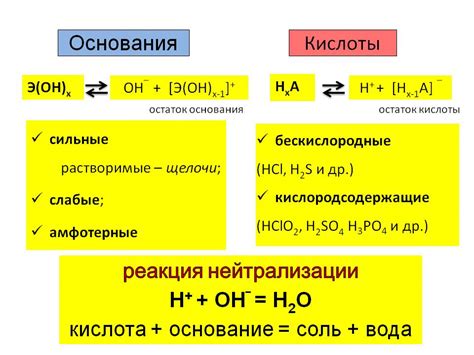
Кислоты - это вещества, способные отдавать протоны (водородные ионы) в растворе. Они обладают кислыми свойствами и считаются электролитами. Кислоты могут быть органическими (например, уксусная, лимонная) и неорганическими (серная, соляная). Кроме того, кислоты могут быть сильными и слабыми в зависимости от их способности отдавать протоны.
Основания - это вещества, способные принимать протоны в растворе. Они обладают щелочными свойствами. Основания также могут быть органическими (например, аммиак) и неорганическими (натриевая гидроксидная, калиевая гидроксидная). Основания также могут быть сильными и слабыми в зависимости от их способности принимать протоны.
Кислоты и основания играют важную роль во многих химических реакциях. Они могут взаимодействовать между собой, образуя соли. Эти реакции называются реакциями нейтрализации. Например, кислота и основание могут образовать соль и воду.
Помимо реакций нейтрализации, кислоты и основания могут принимать участие в других типах реакций, например, окислительно-восстановительных реакциях и реакциях образования осадков.
Для успешной сдачи ОГЭ по химии необходимо знать основные свойства кислот и оснований, способы их классификации и взаимодействия, а также уметь применять полученные знания на практике. Подготовка к экзамену должна включать изучение теоретического материала, выполнение практических заданий и решение тестовых задач.
Термодинамика
Тема "Термодинамика" включает в себя изучение законов, принципов и процессов, связанных с теплом и энергией. Важно основательно подготовиться к этой теме, так как она составляет значительную часть программы по химии для ОГЭ.
Основные темы, которые необходимо изучить:
- Термические явления и свойства веществ: расширение вещества при нагревании и сужение при охлаждении;
- Постоянные термические явления: испарение, кристаллизация, плавление и замерзание;
- Изучение фазовых диаграмм с использованием графиков;
- Тепловое равновесие и главный принцип термодинамики;
- Измерение и вычисление значений теплоты и энтальпии;
- Молекулярные и классические представления об энергии;
- Работа в газовых процессах.
При подготовке к ОГЭ по химии, важно уделить особое внимание пониманию основных понятий и законов термодинамики. Определения и формулы помогут вам уяснить закономерности и взаимосвязи в этой области.
Советы для успешной подготовки:
1. Изучайте теорию с пояснениями и примерами. Попробуйте объяснить каждое понятие своими словами и применить его на практике.
2. Работайте с задачами и упражнениями. Только практическая отработка позволит вам усвоить материал и научиться его применять.
3. Используйте учебники и онлайн-ресурсы. Дополнительные источники информации помогут более глубоко понять тему и дадут возможность найти разные подходы к решению задач.
4. Регулярно повторяйте и закрепляйте материал. Повторение является важным этапом запоминания и укрепления знаний.
5. Задавайте вопросы. Если у вас возникают трудности или непонятные моменты, не стесняйтесь обратиться за помощью к учителю или товарищам по учебе.
Следуя этим рекомендациям и тщательно подготовившись к теме "Термодинамика", вы будете готовы к успешной сдаче ОГЭ по химии.
Электрохимия

Электролиты - это вещества, способные проводить электрический ток в жидком или растворенном состоянии. Они могут быть как ионными (состоять из положительно и отрицательно заряженных ионов), так и молекулярными (не имеющими заряда).
Электроды - это проводники, которые используются для подачи и сбора электрического тока в химической реакции. Они могут быть разделены на два типа: аноды (положительно заряженные) и катоды (отрицательно заряженные).
Электролиз - процесс разложения вещества под воздействием электрического тока. При электролизе происходит перенос заряда через электролит, что приводит к химическим реакциям на электродах.
Гальванические элементы - устройства, преобразующие химическую энергию в электрическую. Они состоят из двух полуэлементов, разделенных электролитом. В гальваническом элементе происходит спонтанная химическая реакция, сопровождающаяся выделением электрического тока.
Изучение электрохимии важно для понимания различных процессов, происходящих в природе и промышленности. Также электрохимические явления широко используются в различных научных и технических областях, включая электроэнергетику, химическую промышленность и медицину.
Органическая химия
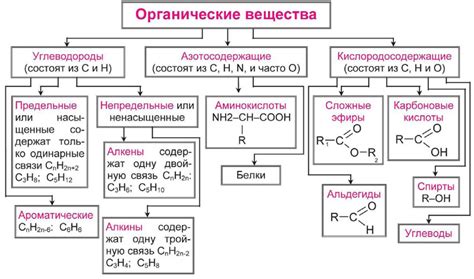
Основные темы органической химии, которые необходимо изучить для успешной сдачи ОГЭ:
- Структура органических соединений.
- Номенклатура органических соединений - правила называния и обозначения органических соединений.
- Функциональные группы - группы атомов, определяющие химические свойства органических соединений.
- Реакции органических соединений - превращения, которые могут происходить с органическими молекулами.
- Химические свойства органических соединений - растворимость, кислотность, основность и другие свойства.
- Полимеры - большие молекулы, состоящие из повторяющихся мономеров.
Для успешной подготовки к ОГЭ по химии необходимо уделить достаточно времени изучению и практическому применению знаний в органической химии. Регулярное повторение материала, решение задач и проведение экспериментов с органическими соединениями помогут укрепить знания и улучшить результаты на экзамене.
Подготовка к ОГЭ по химии

Сдача ОГЭ по химии требует тщательной подготовки. Правильная организация процесса обучения поможет максимально эффективно использовать время и достичь хороших результатов. В этом разделе мы рассмотрим несколько основных шагов, которые помогут вам успешно подготовиться к ОГЭ по химии.
1. Изучение теоретических основ
Важно начать свою подготовку с изучения теории. ОГЭ по химии включает в себя различные темы, от атомной структуры до органической химии. Почитайте учебник и проанализируйте основные темы с помощью конспектов и схематических таблиц. Важно не только запомнить факты, но и понять основные принципы и взаимосвязи между ними.
2. Решение практических задач
ОГЭ по химии включает раздел с практическими заданиями, включающими в себя расчеты, построение графиков и эксперименты. Регулярно решайте практические задачи, чтобы научиться применять полученные знания на практике. Используйте примеры из учебника или интернет-ресурсов, чтобы больше понять методику расчетов.
3. Прохождение испытания на прочность
Для полноценной подготовки к ОГЭ по химии необходимо пройти испытание на прочность. Регулярные полноформатные тестирования помогут вам привыкнуть к формату экзамена и оценить свои знания. Запишите результаты тестов, чтобы отслеживать свой прогресс и определить наиболее слабые места.
| Подводя итоги | Советы |
|---|---|
| Профессиональная преподавательская помощь на etutorium.ru | Регулярная практика и закрепление материала |
| Использование дополнительных учебных материалов и ресурсов | Составление плана и распределение времени подготовки |
| Повторение и систематизация полученных знаний | Уверенность и вера в свои силы |



